Vaccine COVID-19 và việc cho con bú: dữ liệu nói gì
Theo các tiêu chuẩn đã thiết lập cho các thử nghiệm lâm sàng, những người mang thai và cho con bú không được đưa vào bất kỳ thử nghiệm nào đối với vaccine COVID-19.
Những người mang thai mắc COVID-19 có nhiều khả năng phải nhập viện hơn những người cùng tuổi nhưng không mang thai. Đó có thể là do cơ thể họ đã làm việc vất vả – tử cung ngày càng lớn đẩy lên trên, làm giảm dung tích phổi và hệ thống miễn dịch bị ức chế để không gây hại cho em bé. Những yếu tố đó không biến mất vào ngày đứa trẻ được sinh ra. Do đó, một số bác sĩ sản khoa nghi ngờ rằng những người đang cho con bú cũng dễ bị nhiễm COVID-19 nghiêm trọng.
Molly Siegel, một bác sĩ sản khoa tại Bệnh viện Đa khoa Massachusetts, đã quyết định tiêm vaccine, sau đó tặng các mẫu sữa mẹ của mình cho các nhà nghiên cứu để phân tích thành phần của nó trong những nghiên cứu đầu tiên. Nhờ Siegel và những người tham gia khác, các nhà khoa học đang bắt đầu hiểu ảnh hưởng của vaccine COVID-19 đối với sữa mẹ.
Kathryn Grey, một chuyên gia y học cho bà mẹ và thai nhi tại Bệnh viện Brigham and Women’s ở Boston, Massachusetts, và các đồng nghiệp của cô đã kiểm tra mức độ hoạt động của vaccine Pfizer – BioNTech và Moderna trong nhóm này. Nghiên cứu được thực hiện trên 131 người tham gia chuẩn bị tiêm vaccine bao gồm bà mẹ đang cho con bú, có thai hoặc không, đã phát hiện ra rằng những người đang cho con bú (bao gồm Siegel và 30 người khác) tạo ra phản ứng kháng thể mạnh mẽ giống như những người không cho con bú1. Nói cách khác: vaccine cũng có lợi cho các bà mẹ đang cho con bú. Nghiên cứu thứ hai của Gaw và nhóm của cô, được đăng trên medRxiv, ủng hộ cho kết quả trên2. Nhóm nghiên cứu đã lấy máu từ 23 người tham gia cho con bú và nhận thấy rằng các kháng thể đối với SARS-CoV-2 tăng lên sau liều thứ hai của họ.
Trước đây, Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (CDC) khuyên các bà mẹ cho con bú không nên tiêm vaccine sốt vàng, có liên quan đến một dạng vi-rút sống, suy yếu, nếu không sẽ có khả năng nhiễm trùng truyền sang trẻ sơ sinh. Vì những trường hợp như vậy, một số dược sĩ và người quản lý vaccine đã khuyến khích các bà mẹ dừng cho con bú sau khi họ được tiêm chủng. Không giống như vaccine sốt vàng da, vaccine COVID-19 không có nguy cơ kích hoạt nhiễm trùng hoạt động. Ngoài ra, vaccine COVID-19 rất khó đi vào sữa mẹ. mRNA được sử dụng trong vaccine Pfizer – BioNTech và Moderna, được thiết kế để phân hủy nhanh đến mức nó không bao giờ rời khỏi các tế bào nơi nó được tiêm. Gaw và các đồng nghiệp của cô đã tiến hành một cuộc kiểm tra an toàn trên mẫu sữa mẹ từ sáu người tham gia trong vòng hai ngày sau khi tiêm vaccine Pfizer – BioNTech hoặc Moderna và không tìm thấy dấu vết của mRNA trong cả hai trường hợp3.
Các nhà nghiên cứu từ lâu đã biết rằng trẻ sơ sinh không sản xuất hiệu quả các kháng thể chống lại vi khuẩn và vi rút có hại; và có thể mất từ ba đến sáu tháng để các kháng thể này phát huy tác dụng. Trong khi COVID-19 thường nhẹ ở dân số trẻ hơn, trẻ nhỏ dưới hai tuổi mắc bệnh có nhiều khả năng phải nhập viện hơn trẻ lớn hơn8. Đó là bởi vì các tiểu phế quản và các đường dẫn khí đến phổi ở trẻ sơ sinh nhỏ hơn rất nhiều. Ngoài ra, trẻ sơ sinh và trẻ em có thể phát triển một căn bệnh nghiêm trọng được gọi là MIS-C (hội chứng viêm đa hệ ở trẻ em), trong đó các bộ phận khác nhau của cơ thể cũng bị viêm sau khi trẻ bị nhiễm COVID-19, có thể gây tử vong.
Sữa mẹ có chứa rất nhiều các kháng thể có khả năng ngăn chặn các mối đe dọa tiềm ẩn đối với trẻ sơ sinh ở giai đoạn đầu này. Các nghiên cứu đã chỉ ra rằng trẻ bú mẹ hoàn toàn trong sáu tháng đầu giúp trẻ hạn chế được một số bệnh như viêm tai giữa5, nhiễm trùng hô hấp6, cúm mùa7 hơn nhiều so với trẻ bú mẹ trong thời gian ngắn hơn hoặc hoàn toàn không bú mẹ. Điều này cũng có thể đúng với kháng thể COVID-19. Đầu năm nay, các nhà nghiên cứu phát hiện ra rằng sữa mẹ từ những người phục hồi sau virus cũng chứa các kháng thể tương tự như vậy8. Và một loạt các nghiên cứu nhỏ, một số chưa đánh giá ngang hàng, đã tìm thấy kháng thể trong sữa mẹ từ những người được tiêm vaccine1,2,9–12
Vào năm 2020, một nhóm nghiên cứu ở Hà Lan đã phát hiện ra các kháng thể từ sữa mẹ của những người bị nhiễm SARS-CoV-2 trước đó có thể vô hiệu hóa vi rút trong phòng thí nghiệm13. Một tháng sau, Young, Jarvinen-Seppo và các đồng nghiệp của họ đã công bố những phát hiện tương tự14. Cả hai nhóm hiện đang thực hiện cùng một thí nghiệm với các kháng thể do vaccine tạo ra, sau một nghiên cứu của các nhà khoa học ở Israel10 cho thấy rằng các kháng thể được tạo ra sau khi tiêm vaccine có thể ngăn chặn virus lây nhiễm vào tế bào và có thể sẽ bảo vệ được em bé.
Nhưng điều này chỉ có thể xảy ra nếu các kháng thể vẫn tồn tại trong một thời gian đáng kể. Một nghiên cứu trên 33 người15 cho thấy rằng việc sản xuất kháng thể ở người lớn được tiêm vaccine Moderna tiếp tục trong ít nhất 6 tháng. Điều đó có thể có nghĩa là trẻ sẽ tiếp tục nhận được một số bảo vệ từ mẹ, miễn là chúng tiếp tục bú mẹ – mặc dù nồng độ kháng thể trong sữa mẹ giảm theo thời gian4.
Nhiều dữ liệu hơn đang được thực hiện. Gray và nhóm của cô ấy sẽ theo dõi những người tham gia của họ, bao gồm Siegel và những người khác, trong suốt một năm (mặc dù các chi tiết vẫn đang được thảo luận). Nhóm của Gaw tại Đại học California, San Francisco, đang lên kế hoạch đánh giá sức khỏe tổng thể và tỷ lệ nhiễm trùng của trẻ sơ sinh khi chúng đang được bú sữa mẹ. Các nhà khoa học cũng đang nghiên cứu để phân tích chi tiết hơn các kháng thể, ví dụ như theo dõi sự tăng trưởng và phát triển của trẻ sơ sinh.
Tuy nhiên, kết quả cho đến nay vẫn đủ hứa hẹn để hầu hết các chuyên gia khuyến khích các bà mẹ đang cho con bú tiêm phòng.
Sữa mẹ chứa tổng nồng độ globulin miễn dịch (Ig) khoảng 0,6mg / mL, chủ yếu ở dạng IgA tiết (90%), khoảng 8% là IgM tiết, 2% còn lại của Ig sữa mẹ là IgG chủ yếu từ huyết thanh16.
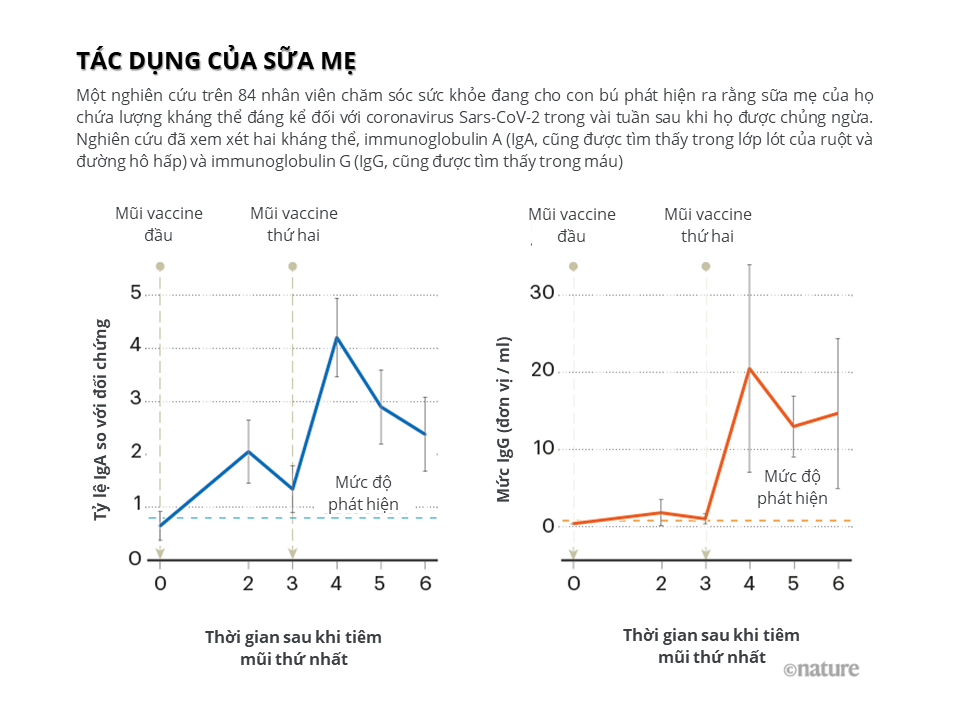
Nguồn: Nature 594, 492-494 (2021); Haia Perl, S. et al. JAMA 325, 2013–2014 (2021).
Nghiên cứu cho thấy kháng thể đặc hiệu IgA và IgG SARS-CoV-2 tiết ra trong sữa rất mạnh trong vòng 6 tuần sau khi tiêm vaccine. IgA tiết ra ngay sau 2 tuần khi tiêm mũi thứ nhất nhưng liều thứ hai không tạo ra loại kháng thể này. Trong khi đó, ở 14 ngày kể từ liều thứ hai, sữa mẹ dường như chủ yếu giàu IgG.
Nghiên cứu khác tại Mỹ đã so sánh thành phần kháng thể trong sữa của 50 bà mẹ đang cho con bú sau khi tiêm chủng với ba loại vaccine của Moderna, Pfizer và J&J. Nhìn chung, mức độ tiết kháng thể do tiêm chủng gây ra là thấp đối với tất cả các loại vaccine. Đáp ứng kháng thể trong sữa mẹ có thể được tăng cường một cách khiêm tốn bởi vaccine Moderna về hiệu giá IgA tiết so với các vaccine khác. Các nhà khoa học nhận định “vaccine J&J kém tạo ra đột biến Ab đặc hiệu trong sữa so với vaccine dựa trên mRNA. Những dữ liệu này cho thấy vaccine Moderna là lý tưởng nhất, trong khi vaccine J&J nên được coi là phương án cuối cùng. Điều này cũng nhấn mạnh sự cần thiết phải phát triển các loại vaccine hiệu quả hơn để sử dụng trong thời kỳ mang thai và cho con bú với mục đích cung cấp mức độ bảo vệ tốt nhất cho trẻ đang bú mẹ16 .

Nguồn: https://doi.org/10.1101/2021.07.19.21260794
Đáp ứng kháng thể sữa đặc hiệu SARS-CoV-2 Spike gây ra bởi vaccine COVID-19. A) Đường cong chuẩn độ IgG (bảng trên) và hiệu giá điểm cuối (bảng dưới). (B) Đường cong chuẩn độ IgA (bảng trên) và hiệu giá điểm cuối (bảng dưới). (C) Đường cong chuẩn độ kháng thể tiết (bảng trên) và hiệu giá điểm cuối (bảng dưới). Các đường chấm cho biết các giá trị ngưỡng dương. Người trả lời (%): Phần trăm người tham gia nhận loại vaccine này có hiệu giá điểm cuối dương tính. **** p <0,0001; * 0,009 <p <0,05. Giá trị trung bình được hiển thị trong biểu đồ phân tán.
Tác giả: Lê Huỳnh Tú Mỹ, Nguyễn Thị Thanh Vân
NGUỒN THAM KHẢO
- Gray, K. J. et al. Preprint at medRxiv https://doi.org/10.1101/2021.03.07.21253094 (2021).
- Golan, Y. et al. Preprint at medRxiv https://doi.org/10.1101/2021.03.09.21253241v2 (2021).
- Golan, Y. et al. Preprint at medRxiv https://doi.org/10.1101/2021.03.05.21252998v1 (2021).
- Atyeo, C. & Alter, G. Cell 184, 1486–1499 (2021).
- Bowatte, G. et al. Acta Paediatr. 104, 85–95 (2015).
- Tromp, I. et al. PLoS ONE 12, e0172763 (2017).
- Zaman, K. et al. N. Engl. J. Med. 359, 1555–1564 (2008).
- Kim, L. et al. Morb. Mortal. Wkly Rep. 69, 1081–1088 (2020).
- Baird, J. K., Jensen, S. M., Urba, W. J., Fox, B. A. & Baird, J. R. Preprint at medRvix https://doi.org/10.1101/2021.02.23.21252328 (2021).
- Rosenberg Friedman, M. et al. Preprint at medRxiv https://doi.org/10.1101/2021.03.06.21252603 (2021).
- Kelly, J. C. et al. Am. J. Obstet. Gynecol. https://doi.org/10.1016/j.ajog.2021.03.031 (2021).
- Haia Perl, S. et al. JAMA 325, 2013–2014 (2021).
- van Keulen, B. et al. Preprint at medRxiv https://doi.org/10.1101/2020.08.18.20176743 (2020).
- Pace, R. M. et al. mBio 12, e03192-20 (2021).
- Doria-Rose, N. et al. N. Engl. J. Med. 384, 2259–2261 (2021).
- https://doi.org/10.1101/2021.07.19.21260794
- https://www.nature.com/articles/d41586-021-01680-x?fbclid=IwAR2gTk0MCy6dc0Xq2VTKLjOSuxWy_0sXW74P3P1mpwtOyzrdKNlrZFtX__A