Cập nhật tình hình phát triển thuốc và vắc xin covid-19 (tính đến 9/2020)
Tác giả: Lâm Trịnh Diễm Ngọc
Mentor: Võ Đức Duy, Ph.D.
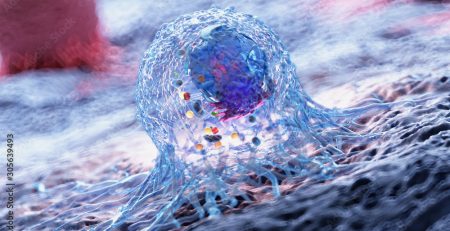
Tính đến ngày 30/9/2020, chỉ trong vòng hơn 6 tháng, dịch corona đã lây nhiễm hơn 33 triệu người và 1 triệu người chết trên khắp thế giới. Để ngăn chặn đại dịch và lịch sử như dịch cúm tây ban nha (1918 spanish flu, hơn 17 triệu người chết) tái diễn, sự phát triển đồng thời vaccine và thuốc càng nhanh càng tốt là điều cấp thiết.
- THUỐC

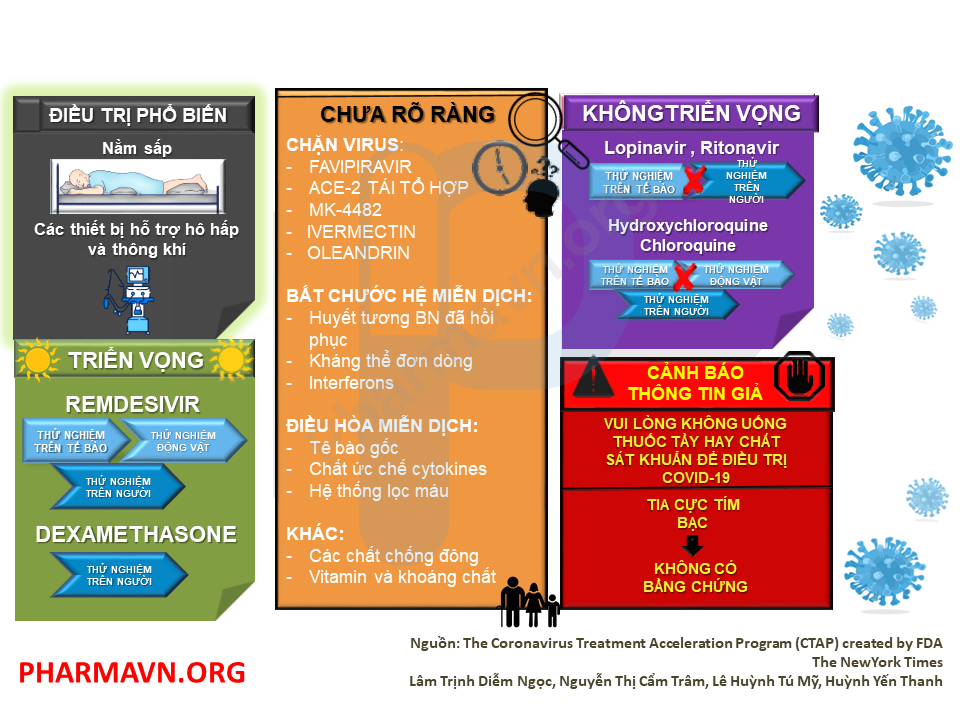
Dưới đây là danh sách các báo cáo mới nhất liên quan đến việc thiết kế và phát triển thuốc điều trị COVID-19.
- 24/9 – Tiến hành thử nghiệm giai đoạn III với REGN-COV2 (hỗn hợp hai kháng thể đơn dòng được phân lập từ bệnh nhân đã khỏi bệnh và từ chuột biến đổi gen) để đánh giá khả năng phòng ngừa nhiễm SARS-CoV-2.
- 23/9 – Phát hiện cơ chế mới của remdesivir: ức chế polymerase của virus ngăn cản quá trình nhân đôi (in vitro)
- 18/9 – 4-Phenylbutiric acid (4-PBA) ngăn chặn hoặc giảm nhẹ hậu quả do nhiễm SARS-CoV-2 bằng cách kiểm soát “cơn bão” cytokine, hạn chế hoàn toàn tỷ lệ tử vong do suy hô hấp (trên mô hình động vật)
- 17/9 – Pfizer đã bắt đầu thử nghiệm lâm sàng giai đoạn I của PF-07304814 (tiêm tĩnh mạch), một phân tử nhỏ chứa 1 nhóm phosphat và bị phân cắt bởi các enzym phosphatase kiềm trong mô, giải phóng hoạt chất PF-00835231. Hợp chất này nhắm vào enzym protease 3CL mà coronavirus sử dụng để tự lắp ráp và nhân lên. Nếu được chấp thuận, PF-07304814 sẽ là loại thuốc kháng virus đầu tiên nhắm vào loại protein này.
PF-00835231 và remdesivir có tác động hiệp đồng, do đó khi phối hợp có thể giảm liều của từng hợp chất.

- 14/9 – Thành phần kháng thể kích thước tí hon Ab8 vô hiệu hóa SARS-CoV-2 trong mô hình động vật
- 14/9 – Hỗn hợp kháng thể REGN-COV2 tiến vào thử nghiệm giai đoạn III.
- 9/9 – Thiết kế những phân tử protein có ái lực cao với spike protein của virus, ức chế sự gắn kết của virus vào tế bào người theo cơ chế cạnh tranh. Trong đó, LCB1 là ứng cử viên hàng đầu với hiệu lực cao hơn gần 6 lần so với các kháng thể đơn dòng hiệu quả nhất được báo cáo cho đến nay (trên mô hình động vật).
- 19/8 – Thống kê 21 loại thuốc có hoạt tính chống lại SARS-CoV-2, chia thành 3 nhóm:
+ Các hợp chất có tác dụng hiệp đồng với remdesivir: SB-616234-A (giai đoạn tiền lâm sàng), MLN-3897 (giai đoạn II), VBY-825 (giai đoạn tiền lâm sàng) và hanfangchin A (tetrandrine – dẫn xuất của chloroquine, giai đoạn III)
+ Các hợp chất ngăn chặn sự nhân lên của virus trong tế bào phổi: apilimod (giai đoạn II), ONO-5334 (đang thử nghiệm giai đoạn II trong điều trị Loãng xương sau mãn kinh) và MDL-28170 (chưa tiến hành thử nghiệm lâm sàng).
+ Các hợp chất đã được FDA chấp thuận (astemizole và clofazimine), cũng như remdesivir gần đây đã nhận được Giấy phép sử dụng khẩn cấp.
- 14/8 – Ebselen ức chế enzym virus tại 2 vị trí, có thể có hiệu quả như một vũ khí chống lại virus corona (giai đoạn II)
- 4/8 – Phát hiện hai thuốc disulfiram (điều trị nghiện rượu) và neratinib (điều trị ung thư vú) có tiềm năng ức chế protease chính “Mpro” của coronavirus qua liên kết cộng hóa trị. Tuy nhiên, neratinib không hiệu quả trên lâm sàng, còn disulfiram đã được đăng ký thử nghiệm lâm sàng giai đoạn II.
- 2/8 – RLF-100 (aviptadil) giúp phục hồi nhanh chóng sau suy hô hấp ở bệnh nhân nặng COVID-19 nặng và ngăn chặn sự sao chép của virus trong tế bào phổi và bạch cầu đơn nhân của người (giai đoạn II).
- 27/7 – LAM-002A (apilimod) tiến vào thử nghiệm giai đoạn II. Các kết quả trước đó cho thấy LAM-002A có thể chống lại nhiễm trùng SARS-CoV-2 trong phổi, hiệp đồng tác dụng với remdesivir.
- 23/7 – Kết quả thử nghiệm trên tế bào: Chiết xuất tảo biển (fucoidan RPI-27 – cấu trúc polysaccarid sulfat hóa) có hoạt tính kháng virus mạnh hơn remdesivir và không gây độc tế bào ngay cả ở nồng độ cao nhất được thử nghiệm.
- 22/7 – Chloroquine ức chế sự lây nhiễm SARS-CoV-2 ở tế bào thận khỉ nhưng KHÔNG ngăn chặn sự xâm nhập của virus này vào các tế bào phổi người.
Chloroquine và/hoặc hydroxychloroquine đã bước vào thử nghiệm giai đoạn II/III tuy nhiên từ tháng 6, các cuộc thử nghiệm của WHO, NIH, Sanofi và Novartis đã ngừng hẳn vì thiếu bằng chứng về tính an toàn và hiệu quả.
- 21/7 – Oxid nitric ức chế sự nhân lên của virus bằng phản ứng gây độc tế bào. Đây là một trong những phương pháp điều trị COVID-19 tiềm năng được đưa vào chương trình tiếp cận mở rộng khẩn cấp của FDA. Liệu pháp điều trị bằng oxid nitric cho bệnh nhận Covid-19 hiện đang được thử nghiệm lâm sàng giai đoạn II.
- 20/7 – SNG001 (công thức interferon beta dạng hít) qua thử nghiệm giai đoạn II cho kết quả tích cực ở bệnh nhân COVID-19 nhập viện: khả năng hồi phục tăng gấp đôi, giảm khó thở, giảm tỷ lệ phát triển bệnh nặng.
- 15/7 – Heparin có thể liên kết với SARS-CoV-2 và là một ứng cử viên đầy hứa hẹn cho chiến lược mồi nhử, hiện đã bước vào thử nghiệm giai đoạn III.
- 14/7 – DAS181 (thuốc kháng virus, dạng phun sương) bước vào thử nghiệm giai đoạn III. Các kết quả trước đó cho thấy thuốc ngăn chặn SARS-CoV-2 xâm nhập đường hô hấp và cải thiện phản ứng miễn dịch của bệnh nhân.
- 11/7 – Liều duy nhất Tocilizumab giảm hơn 45% tỉ lệ tử vong ở bệnh nhân COVID-19 sử dụng máy thở nhưng làm tăng tỉ lệ bội nhiễm, được đề xuất dự phòng thay cho dexamathason ở bệnh nhân gặp bất lợi với liệu pháp steroid (giai đoạn III).
Tuy nhiên sau đó vào ngày 29/7, một thử nghiệm lâm sàng khác ở giai đoạn III được tiến hành bởi hãng La-Roche công bố kết quả không khả quan rằng Tocilizumab không giúp cải thiện tỉ lệ tử vong, đặt dấu chấm hỏi về lợi ích của thuốc này trên bệnh nhân COVID-19.
- 4/7 – WHO NGỪNG thử nghiệm lâm sàng hydroxychloroquine và lopinavir / ritonavir vì làm giảm ít hoặc không làm giảm tỷ lệ tử vong ở bệnh nhân COVID-19 nhập viện.
- 29/6 – Kết quả thử nghiệm RECOVERY: Lopinavir-Ritonavir KHÔNG mang lại lợi ích lâm sàng cho bệnh nhân COVID-19 nằm viện.
- 30/6 – TAT CARMIL1 (sự kết hợp của hai peptit có nguồn gốc tự nhiên) làm giảm phản ứng viêm cấp tính (ex vivo)
- 30/6 – Dạng triphosphat của sofosbuvir có thể chấm dứt phản ứng polymerase, ngăn chặn sự phát triển của virus. Ngoài ra, sofosbuvir và dạng triphosphat của alovudine, zidovudine, tenofovir alafenamide và emtricitabine cũng ức chế polymerase SARS-CoV-2 với các mức hiệu quả khác nhau (in vitro)
- 25/6 – Thử nghiệm alpha-1-antitrypsin ở bệnh nhân COVID-19 nặng được thở máy trong ICU với hội chứng rối loạn hô hấp cấp. Đây là thử nghiệm “Điều tra sản phẩm Thuốc” đầu tiên được phê duyệt ở Ireland để thử nghiệm một liệu pháp điều trị COVID-19 (giai đoạn II).
- 25/6 – Remdesivir là loại thuốc đầu tiên chống lại COVID-19 được khuyến nghị cấp phép ở EU.
- 24/6 – Baricitinib có thể làm giảm viêm và tải lượng virus SARS-CoV-2. Hãng Eli Lilly and Company đã tiến hành thử nghiệm lâm sàng giai đoạn III với
- 22/6 – Canakinumab, một chất chẹn interleukin-1 (IL-1), bước vào thử nghiệm giai đoạn III để đánh giá tác dụng ngăn ngừa hội chứng giải phóng cytokine (CRS) ở bệnh nhân viêm phổi COVID-19.
- 16/6 – Kết quả thử nghiệm RECOVERY: Dexamethasone là loại thuốc đầu tiên làm giảm tỷ lệ tử vong do COVID-19 với liều thử nghiệm 6 mg/lần/ngày (PO hoặc IV).
- 15/6 – Kết quả thử nghiệm in vitro: Bốn ứng cử viên nhắm mục tiêu vào enzym protease “Mpro” của virus gồm Boceprevir (thuốc điều trị Viêm gan C), chất ức chế calpain II và XII (ức chế đồng thời Mpro và calpain / cathepsin), GC-376 (một loại thuốc thú y, hiệu quả nhất trong 4 hợp chất, đang chuẩn bị thử nghiệm lâm sàng).
(ở người không có enzym Mpro nên các loại thuốc nhắm vào enzym này sẽ đặc hiệu và ít gây ra tác dụng phụ hơn)
- 8/6 – Hơn 2000 thử nghiệm lâm sàng đối với phương pháp điều trị COVID-19 tiềm năng đã được đăng ký.
- 1/6 – Kết quả thử nghiệm SIMPLE (giai đoạn III): Nhóm dùng remdesivir 5 ngày có khả năng cải thiện lâm sàng ở ngày thứ 11 cao hơn 65% so với những bệnh nhân trong nhóm chăm sóc tiêu chuẩn.
- 1/5 – FDA ban hành Giấy phép Sử dụng Khẩn cấp (EUA) cho remdesivir để điều trị bệnh nhân nhập viện với COVID-19 nặng qua đường tĩnh mạch.
- VẮC XIN
Tính đến tháng 8/2020, có hơn 180 vắc xin chống lại virus SARS-CoV-2 đang được nghiên cứu phát triển. Dưới đây là danh sách 34 vắc xin mới nhất đang được thử nghiệm lâm sàng trên người và tiến trình thử nghiệm của chúng tính đến ngày 3/9.
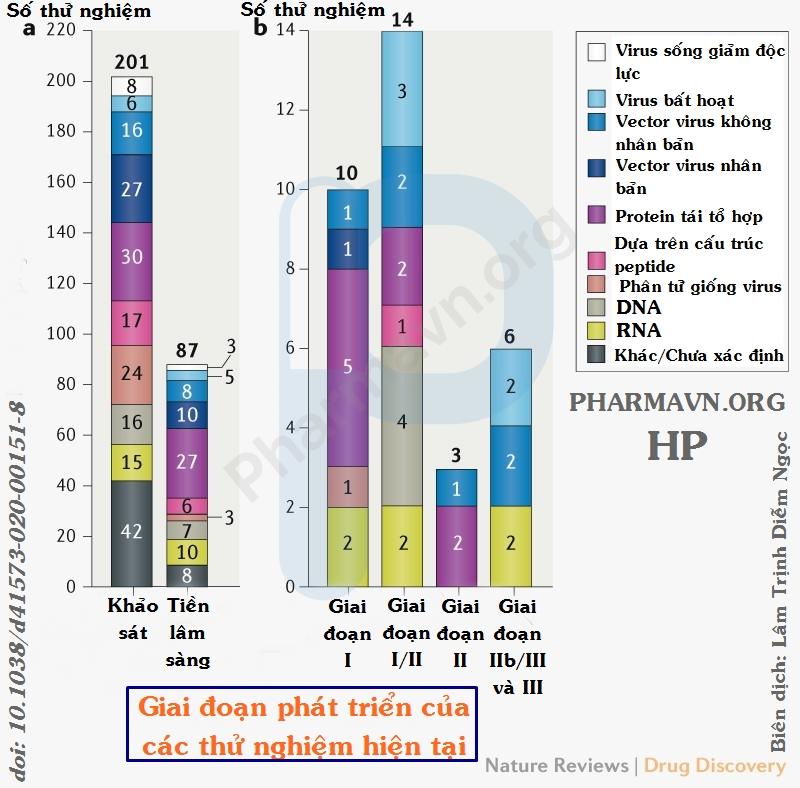
- AZD1222 (trước đó gọi là ChAdOx1 nCov-19) – Giai đoạn I/II, III (Anh)
AZD1222 là vắc xin adenovirus tái tổ hợp được phát triển bởi AstraZeneca, Đại học Oxford và Vaccitech. Kết quả thử nghiệm giai đoạn I / II (1000 người tham gia) chứng minh rằng vắc xin này có thể tạo ra phản ứng tế bào T trong vòng 14 ngày kể từ ngày tiêm chủng, bên cạnh phản ứng kháng thể trong vòng 28 ngày.
AZD1222 gần đây đã bước vào thử nghiệm giai đoạn III.
- Ad5-nCoV – Giai đoạn I,II, III (Trung Quốc)
Ad5-nCoV được phát triển bởi CanSino Biologics Inc. và Viện Công nghệ Sinh học Bắc Kinh, được xây dựng dựa trên nền tảng vắc xin adenovirus từng được sử dụng cho các bệnh truyền nhiễm như Ebola.
Kết quả thử nghiệm giai đoạn II chứng minh rằng hai liều vắc-xin được tiêm khác nhau đã tạo ra phản ứng trung hòa của kháng thể chống lại SARS-CoV-2 một cách đáng kể, không có phản ứng bất lợi nghiêm trọng nào được ghi nhận.
- Gam-COVID-Vac Lyo – Giai đoạn I, III (Nga)
Vắc xin “Gam-COVID-Vac” do Viện Gamaleya của Moscow phát triển dựa trên adenovirus (tương tự AZD1222) đã bước vào thử nghiệm lâm sàng giai đoạn I vào tháng 6 với 38 người tham gia khỏe mạnh. Theo hồ sơ nghiên cứu thử nghiệm lâm sàng của Viện Y tế Quốc gia, thử nghiệm này vẫn đang tiếp tục.
Tuy nhiên, vào ngày 1/8, các phương tiện truyền thông Nga đưa tin rằng Bộ trưởng Bộ Y tế Nga Mikhail Murashko tuyên bố rằng “Các thử nghiệm lâm sàng về vắc xin coronavirus do Trung tâm Gamaleya phát triển đã kết thúc, thủ tục giấy tờ đang được tiến hành để đăng ký vắc xin”. Đến nay, Nga chưa công bố bất kỳ dữ liệu khoa học nào liên quan đến Gam-COVID-Vac.
- mRNA-1273 – Giai đoạn I, II, III (Anh)
“mRNA-1273” là vắc xin mRNA mã hóa cho protein S (spike protein) của virus, được phát triển bởi Moderna Inc. Thử nghiệm pha I cho kết quả tích cực: kháng thể liên kết với protein S tăng đột biến ở tất cả những người tham gia sau lần tiêm chủng đầu tiên.
Gần đây, Moderna thông báo rằng công ty đang thảo luận với Bộ Y tế, Lao động và Phúc lợi Nhật Bản về việc mua hơn 40 triệu liều mRNA-1273 để hỗ trợ chiến lược tiêm chủng càng sớm càng tốt cho người dân nước này.
- CoronaVac – Giai đoạn I/II, II, III
CoronaVac là vắc xin SARS-CoV-2 bất hoạt, được phát triển bởi công ty Trung Quốc Sinovac Biotech, Nghiên cứu giai đoạn I / II (với 743 người tham gia) cho thấy CoronaVac an toàn và có thể tạo ra phản ứng miễn dịch. Kết quả thử nghiệm giai đoạn III (với gần 10000 người tham gia) dự kiến có được trong tháng 11 tới.
Với tiến độ này, Sinovac gần như chẳng hề kém cạnh các hãng dược phương Tây như AstraZeneca và Moderna trong cuộc đua phát triển vắc xin COVID-19.
- Chương trình vắc xin BTN162 – Giai đoạn I/II, III
Pfizer đang hợp tác với công ty BioNTech của Đức về chương trình vắc xin COVID-19 được gọi là BTN162 để tiến hành thử nghiệm một số vắc xin mRNA. Tính đến hiện tại, ứng cử viên hàng đầu của họ là BTN162b2.
Những dữ liệu ban đầu cho thấy khả năng sinh miễn dịch và tính an toàn đầy hứa hẹn. Pfizer và BioNTech hy vọng nhận được sự chấp thuận của cơ quan quản lý sớm nhất là vào tháng 10/2020 với kế hoạch cung cấp 100 triệu liều trên toàn quốc vào cuối năm 2020 và khoảng 1,3 triệu liều vào cuối năm 2021.
Danh sách các vắc xin từ 7 – 34 được tóm tắt trong bảng sau.
| STT | Vắc-xin | Nhà sản xuất | Giai đoạn |
| 7 | NVX CoV2373 | Novavax | I/II, II |
| 8 | GRAd-COV2 | ReiThera, LEUKOCARE và Univercells | I |
| 9 | INO-4800 | Inovio Pharmaceuticals và Viện Vắc xin quốc tế | I/II |
| 10 | LNP-nCoVsaRNA | Cao đẳng Hoàng gia Luân Đôn | I |
| 11 | Vắc xin dựa trên protein tái tổ hợp có tá dược bổ trợ | Sanofi Pasteur và GSK | I/II
(Các nghiên cứu tiền lâm sàng cho thấy tính an toàn và khả năng sinh miễn dịch đầy hứa hẹn) |
| 12 | Vắc xin mRNA | CureVac | I, II |
| 13 | Vắc xin virus n-CoV bất hoạt | Viện Sản phẩm Sinh học Vũ Hán và Sinopharm | I/II, III |
| 14 | Vắc xin virus n-CoV bất hoạt | Viện Sản phẩm Sinh học Bắc Kinh và Sinopharm | I/II, III |
| 15 | Vắc xin virus SARS-CoV-2 bất hoạt | Học viện Khoa học Y học Trung Quốc | I, II |
| 16 | Protein tái tổ hợp có tá dược bổ trợ
(RBD-Dimer) |
Anhui Zhifei Longcom Biopharmaceutical, Viện Vi sinh vật và Viện Hàn lâm Khoa học Trung Quốc | I, II |
| 17 | Vắc xin DNA plasmid | Đại học Osaka, AnGes và Takara Bio | I/II |
| 18 | Vắc xin dựa trên miền liên kết thụ thể | Kentucky Bioprocessing | I/II |
| 19 | Vắc xin S-trimer | Clover Biopharmaceuticals, GSK và Dynavax | I |
| 20 | Protein gai (spike protein) tái tổ hợp với tá dược Advax™ | Vaxine Pty và Medytox | I |
| 21 | Vắc xin DNA (GX-19) | Genexine Consortium | I/II |
| 22 | Vắc xin bất hoạt toàn bộ virion | Bharat Biotech | I/II |
| 23 | Vắc xin DNA plasmid | Cadila Healthcare | I/II |
| 24 | Kìm giữ phân tử (molecular clamp) được ổn định bởi protein S và tá dược MF59 | Đại học Queensland, CSL và Seqirus | I |
| 25 | VLP có nguồn gốc thực vật được bổ trợ tá dược GSK hoặc Dynavax | Medicago | I |
| 26 | Vắc xin mRNA | Viện Hàn lâm Khoa học Quân sự Trung Quốc và Walvax Biotech | I |
| 27 | Ad26COVS1 | Công ty dược phẩm Janssen | I/II, III (chưa triển khai) |
| 28 | mRNA | Arcturus/Duke-NUS | I/II |
| 29 | Vector virus nhân bản | Viện Pasteur, Themis, Đại học Pittsburgh CVR và Merck Sharp & Dohme | I |
| 30 | RBD (sự sản xuất baculovirus biểu hiện trong các tế bào Sf9) | Bệnh viện Tây Trung Quốc và Đại học Tứ Xuyên | I |
| 31 | Vắc xin peptide | FBRI SRC VB VECTOR, Rospotrebnadzor, Koltsovo | I |
| 32 | Vắc xin tiểu đơn vị protein | Viện vắc xin Finlay, Cuba | I |
| 33 | Vắc xin tiểu đơn vị với Dynavax’s CpG 1018 | Medigen Vaccine Biologics Corporation/NIAID/Dynavax | I |
| 34 | Vắc xin bất hoạt | Viện nghiên cứu các vấn đề an toàn sinh học, Đại diện của Kazakhstan | I/II |
TLTK:
- https://www.technologynetworks.com/drug-discovery/articles/stay-up-to-date-with-covid-19-drug-development-337641?fbclid=IwAR3TiyyLdkZBLBp57jgGz3SghOpCYELuzEWTdEpqKOHSmJwiWtx2WxSJ7gk
- https://cen.acs.org/pharmaceuticals/drug-discovery/Pfizers-novel-COVID-19-antiviral/98/web/2020/09?fbclid=IwAR05kDTGN2znn3GUFfRskrCpAGOtUSalcvQKUjrvyuCesW9DeIUcs2nl1Ps
- https://www.technologynetworks.com/biopharma/blog/which-covid-19-vaccines-are-in-human-clinical-trials-337816
- https://pharmavn.org/vaccine-chong-covid-19-cuoc-dua-tu-ma.html
- https://www.thelancet.com/journals/lanrhe/article/PIIS2665-9913(20)30313-1/fulltext
- https://www.fiercepharma.com/pharma/end-road-for-hydroxychloroquine-covid-19-as-novartis-nih-and-who-pull-out-trials
- https://www.rcsi.com/dublin/news-and-events/news/news-article/2020/06/rcsi-begins-clinical-trial-for-potential-drug-therapy-for-severe-covid-19-infection?fbclid=IwAR2plbqWg3Joct15VT8GsC9leSre2c9kku8w-sJMA8KKD2SK3gyoGXz_FXo