Bệnh Chikungunya và virus Chikungunya
Biên dịch: Nguyễn Việt Nhựt Quang, Trương Hoàng Thiện, Đặng Thị Trâm
Mentor: Võ Đức Duy, Ph.D.
Tổng Quan:
Vi rút Chikungunya là một loại vi rút RNA thuộc giống alphavirus của họ Togaviridae, có thể lây sang người qua vết đốt của muỗi mang bệnh. Các triệu chứng phổ biến nhất của nhiễm trùng là sốt và đau khớp. Ngoài ra, các triệu chứng khác có thể bao gồm nhức đầu, đau cơ, sưng khớp hoặc phát ban.
Các đợt bùng phát đã xảy ra ở các nước Châu Phi, Châu Á, Châu Âu và Ấn Độ Dương và Thái Bình Dương. Mặc dù, vi rút chikungunya lần đầu tiên được xác nhận từ năm 1952 tại miền nam Tanzania, đến cuối năm 2003 những ca nhiễm bệnh bùng nổ và được ghi nhận ở châu Mỹ trên các hòn đảo ở Caribe. Có nguy cơ vi-rút sẽ được du nhập vào các khu vực mới bởi những du khách bị nhiễm bệnh.
Không có thuốc chủng ngừa hoặc thuốc để điều trị nhiễm vi-rút chikungunya. Du khách có thể tự bảo vệ mình bằng cách phòng tránh muỗi đốt. Khi đi du lịch đến các quốc gia có vi rút chikungunya, hãy sử dụng thuốc chống côn trùng, mặc áo dài tay và quần dài, và ở những nơi có máy điều hòa nhiệt độ hoặc sử dụng cửa sổ và cửa ra vào.
- Triệu chứng:
Hầu hết những người bị nhiễm vi rút chikungunya sẽ phát triển một số triệu chứng. Các triệu chứng thường bắt đầu từ 3-7 ngày sau khi bị muỗi mang bệnh cắn.
Phổ biến nhất là sốt và đau khớp. Các triệu chứng khác có thể bao gồm nhức đầu, đau cơ, sưng khớp hoặc phát ban.
Bệnh Chikungunya thường không dẫn đến tử vong, nhưng các triệu chứng có thể nghiêm trọng và gây tàn phế. Hầu hết bệnh nhân cảm thấy tốt hơn trong vòng một tuần. Ở một số người, cơn đau khớp có thể kéo dài trong nhiều tháng.
Những người có nguy cơ cao chuyển biến bệnh nặng hơn ở trẻ sơ sinh, người lớn tuổi (≥65 tuổi) và những người mắc các bệnh lý như huyết áp cao, tiểu đường hoặc bệnh tim, nhưng rất hiếm trường hợp báo cáo tử vong.
Khi người đã bị nhiễm bệnh có khả năng cao sẽ không bị tái nhiễm trong tương lai.
- Chẩn đoán:
Các triệu chứng của bệnh chikungunya tương tự như của bệnh sốt xuất huyết và Zika, các bệnh khác cũng gây ra bởi cùng một loại muỗi mang vi rút chikungunya.
Nếu gặp các triệu chứng được mô tả ở trên và đã đến thăm một khu vực nơi phát hiện thấy chikungunya, nên đi xét nghiệm và cung cấp lịch trình du lịch.
Bác sĩ có thể yêu cầu xét nghiệm máu để tìm chikungunya hoặc các loại vi rút tương tự khác như sốt xuất huyết và Zika.
- Phân bố:
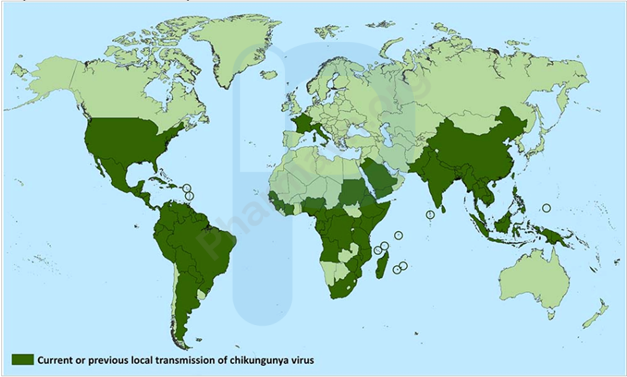
Hình 1. Bản đồ các nước đã và đang có xuất hiện lây nhiễm bệnh Chikungunya. (as of September 17, 2019) – Credits: Geographic Distribution/ Centre of Disease Control and Prevention
- Giải thích cơ chế lây nhiễm của bệnh Chikungunya:
Muỗi Aedes là vector quan trọng các bệnh gây ra bởi arboviruses, chẳng hạn như Chikungunya. Loài truyền bệnh chính của những virus này là Aedes aegypti và Ae. albopictus, hiện diện nhiều ở vùng nhiệt đới và hầu như tất cả trên các nơi trên thế giới. Nghiên cứu về đặc điểm cơ bản của vector này cần thiết để biết về sự lây truyền của vi rút.
Chỉ muỗi cái là có khả năng để truyền qua vật chủ vì chúng là loài hút máu. Ngoài ra, mỗi hệ vi sinh vật về cơ bản sẽ thể hiện lây nhiễm vi rút khác nhau. Vi sinh vật có thể điều chỉnh lượng virus truyền từ muỗi, ví dụ như các vi khuẩn chi Wolbachia có khả năng của việc ngăn chặn virus lây nhiễm, hoặc sinh vật đơn bào của các loài Ascogregarina lại có khả năng của tạo điều kiện vi rút truyền giữa muỗi và ấu trùng.
Các đặc điểm sinh học của muỗi thể hiện khả năng lây truyền của các vi rút vào vật chủ, vì trong dịch chứa nhiều chất có hiệu ứng sinh học, ví dụ như chất điều hòa miễn dịch và chất chống đông máu và khả năng quyết định các tương tác của vật chủ đối với vi rút, can thiệp vào khả năng gây bệnh và độc lực của nó. Thông tin về các vectơ Aedes chikungunya đóng vai trò quan trọng trong việc tìm kiếm các phương pháp mới chống các loại vi rút lây truyền.
- Tương tác giữa vi rút và vectơ mang bệnh:
Vectơ lây truyền theo chiều dọc xảy ra thông qua trứng bị vi rút và vectơ lây truyền theo chiều ngang xảy ra trong lúc hút máu vật chủ. Ban đầu, vi rút tồn tại và nhân lên trong các tế bào midgut (midgut cells) trước khi phân bố đến tế bào máu và tuyến nước bọt trong giai đoạn phơi nhiễm trong vectơ (Coffey et al., 2014). Vi rút cần phải xâm nhập vào lớp nền của tế bào sản xuất nước bọt (acinar cells) để sinh sôi, rồi phân bố và lưu trữ tại nước bọt.
Ở muỗi, các tuyến nước bọt có tính lưỡng cực (sexually dimorphic) và được hình thành bởi cấu trúc ba thùy đặc biệt. Các thùy này bao gồm một lớp nền được bao bọc bởi một lớp biểu mô đơn lẻ hoặc các tế bào sản xuất nước bọt, xung quanh ống dẫn nước bọt trung tâm là nơi nước bọt được giữ lại và sau đó được tiêm vào vật chủ ( Juhn và cộng sự, 2011; Melo và cộng sự ., 2015; Vega và cộng sự, 2015) (Hình 1).
Ngoài ra, trong một thí nghiệm cho muỗi ở giai đoạn trứng rụng sống trong môi trường ấu trùng với một số vi sinh vật. Do đó, chúng chứa nhiều vi sinh vật có thể phát triển và cư trú trong các mô, đặc biệt là trong hệ tiêu hóa, ảnh hưởng đến các chức năng sinh lý, chẳng hạn như trôi đổi dinh dưỡng, tiêu hóa và sinh sản ( Gaio và cộng sự, 2011). Ngoài ra, hệ vi sinh vật này có thể ảnh hưởng đến khả năng gây bệnh cho người (Hegde et al., 2015). Một số nghiên cứu xác định đường tiêu hóa là cấu trúc đầu tiên chịu ảnh hưởng của vi sinh vật, vì đây là cơ quan tiếp nhận và bắt đầu xử lý vật chất ăn vào (Franz và cộng sự, 2015). Khi ở trong cơ thể muỗi, hệ vi sinh vật này có thể can thiệp vào mối quan hệ véc tơ – vật chủ – vi sinh vật (Weaver và Reisen, 2010; Dennison và cộng sự, 2014).
Về vấn đề này, Hegde et al. (2015) đã báo cáo rằng một tương tác có thể diễn ra với cùng một mô hoặc protein đích của arbovirus, với chính virus hoặc thậm chí cả hai, tùy thuộc vào vị trí. Ngoài ra, sự biến đổi của hệ vi sinh vật trong muỗi được điều chỉnh bởi chế độ ăn uống, giới tính, loài và giai đoạn sống.
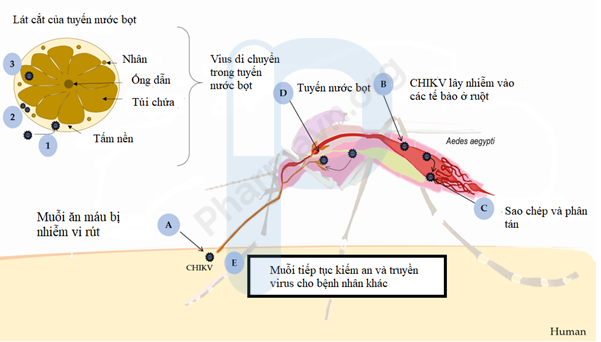
Hình 2. Sự nhân lên của virus trong muỗi.
(A) Muỗi ăn máu bị nhiễm vi rút và xảy ra thời kỳ ủ bệnh nội tại trong vectơ, (B) vi rút lây nhiễm vào các tế bào, (C) sao chép và phân tán đến các cơ quan khác, chẳng hạn như (D) tuyến nước bọt. (1) Nó thâm nhập vào lớp nền của các tuyến nước bọt tế bào xung quanh; (2) sao chép bên trong các tế bào này; và (3) được lắng đọng vào các khoang trên đỉnh, (E) nơi lưu trữ nước bọt của muỗi trước khi tiết ra trong quá trình kiếm ăn. Hình 2 sử dụng các yếu tố từ www.servier.com.
5.2. Vai trò miễn dịch của Aedes sp. về nhiễm trùng vi rút:
Nhiều nghiên cứu cho thấy tác dụng của Aedes bởi các thành phần có trong nước bọt của loài côn trùng và vai trò của chúng trong lây truyền mầm bệnh (Styer và cộng sự, 2011; Surasombatpattana và cộng sự, 2012; Ockenfels và cộng sự, 2014).
Gần đây, nghiên cứu cho thấy rằng Ae. aegypti có thể cải thiện sự tồn tại của nhiễm trùng đa vi khuẩn ở chuột qua việc điều chỉnh dòng chảy bạch cầu trung tính và tăng khả năng chống oxy hóa (Souza Gomes và cộng sự, 2018). Tuy nhiên, hầu hết các nghiên cứu đều báo cáo rằng các thành phần của nước bọt muỗi hoặc bọ chét tạo điều kiện thuận lợi cho quá trình sinh bệnh của vi rút, và cải thiện sự nhân lên của nó (Schneider và Higgs, 2008). Tuyến nước bọt của muỗi sản xuất và tiết ra các loại phân tử (ví dụ, NADH ubiquinone glutathione s-transferase, peroxidase, thioredoxin, cytochrome oxidase) hỗ trợ tiêu hóa đường và mật hoa làm thức ăn của chúng (Ribeiro và Arca, 2009; Ribeiro et al ., 2010); điều này có thể ảnh hưởng đến sự co thắt mạch máu, đông máu, kết tập tiểu cầu (Schneider và Higgs, 2008; Ribeiro và Arca, 2009; Ribeiro và cộng sự, 2010), protein D7 (Calvo và cộng sự, 2009; Ribeiro và cộng sự, 2016) và Sialokinin , điều chỉnh khả năng miễn dịch của vật chủ (Schneider et al., 2004; Wichit et al., 2016).
Aedes có thành phần tuyến nước bọt có thể thay đổi theo môi trường vi mô cục bộ để tạo điều kiện thuận lợi cho việc lây nhiễm arbovirus (Dhawan và cộng sự, 2017).
Một số nghiên cứu báo cáo rằng muỗi mang vi rút có sự thay đổi thành phần của protein tuyến nước bọt , chẳng hạn như: inosine-uridine giả định tương thích nucleoside hydrolase, protein tương tự chất gây dị ứng 30 kDa , serpin và các biến thể protein giống angiopoietin ( Tchankouo-Nguetcheu et al., 2012 ; Shrinet , 2018). SRPN26, protein disulfide-isomerase, chuỗi beta tubulin, enzym malic được điều chỉnh giảm khi có sự hiện diện của vi rút ( Shrinet , 2018). Một số protein được điều chỉnh với tác dụng điều hòa miễn dịch có vai trò trong việc truyền vi rút. Ví dụ, một số protein được tìm thấy trong nước bọt của Aedes có điểm tương tự như nucleoside hydrolase của các loài côn trùng khác, chẳng hạn như giả thuyết inosine-uridine tương thích enzyme nucleoside hydrolase; ưu tiên xúc tác quá trình thủy phân inosine và uridine, và được tăng lên trong tuyến nước bọt của muỗi cái, đóng một vai trò trong việc cung cấp máu cho chúng (Ribeiro và Valenzuela, 2003).
Các nucleosidase trong nước bọt của muỗi cùng với adenosine deaminase (ADA) được tìm thấy ở nước bọt Aedes ngăn chặn sự phân hủy tế bào lớn bằng cách chuyển đổi adenosine thành hypoxanthine, chất này cũng ức chế sản xuất cytokine gây viêm, prostanoids và leukotriene C4. Bên cạnh đó, ADA tạo ra inosine, ức chế sản xuất các cytokine gây viêm, làm giảm phản ứng của vật chủ khi bị hút máu (Ribeiro và Valenzuela, 2003; Ribeiro et al., 2007; Tchankouo-Nguetcheu et al., 2012). Protein tương tự chất gây dị ứng 30 kDa ( Aed a 3), còn được gọi là Aegyptin , ức chế sự kết dính và kết tập tiểu cầu (Chagas et al., 2014). Protein này nhận biết các vị trí liên kết cụ thể là Integrarin a2b1, glycoprotein IV và yếu tố Von Willebrand ( Armiyanti et al., 2015; Peng et al., 2015). Dạng phân tử thấp (41 kDa ) của serpin (chất ức chế serine proteinase) là một protein khác được điều hòa ở tuyến nước bọt của Aedes bị nhiễm CHIKV ( Tchankouo-Nguetcheu et al., 2012). Serpin ức chế các protease nội sinh, chẳng hạn như các protease serine tham gia điều hòa đông máu như yếu tố Xa và thrombin ( Wasinpiyamongkol và cộng sự, 2010). Về mặt này, Serpin tạo điều kiện thuận lợi cho việc lấy máu của muỗi và do đó tăng cường sự lây truyền mầm bệnh từ muỗi sang vật chủ ( Oktarianti và cộng sự, 2015). Tác dụng điều hòa miễn dịch của nước bọt Aedes trong quá trình lây truyền vi rút liên quan đến cảm ứng cục bộ hóa học và phân cực Th2 phân cực Th1 (Boppana et al., 2009). Bên cạnh những protein này được điều chỉnh trong vi rút, tuyến nước bọt của Aedes thể hiện khả năng điều hòa cytokine Th1/Th2 (Schneider và cộng sự, 2004). Một nghiên cứu được thực hiện bởi Thangamani et al. (2010) đã quan sát thấy sự khác biệt về đáp ứng miễn dịch của nhiễm CHIKV bằng phương pháp cấy kim so với khi bị muỗi đốt. Sự lây nhiễm khi có sự hiện diện của nước bọt của muỗi sẽ điều chỉnh phản ứng Th2 với cơ chế điều hòa tăng IL-4 và IL-10 ( Venugopalan et al., 2014). Ngoài ra, cấu hình Th1 cũng được điều chỉnh giảm sau khi tiếp xúc với nước bọt, làm giảm mức IL-2 và IFN-g, và sự biểu hiện của TLR-3. Hơn nữa, muỗi đốt bị nhiễm và không bị nhiễm trùng làm giảm biểu hiện của các thụ thể giống Toll. Lớp tế bào T chuyển sang kiểu hình Th2 trong 6 giờ đầu tiên sau khi được cấy và một số lượng cao bạch cầu trong khu vực tiêm (Thangamani và cộng sự, 2010).
Mặt khác, sự tăng sinh của các tế bào lympho bị suy giảm mạnh. Quả thực là tác dụng của Ae. aegypti về sự tăng sinh và sinh học tế bào lympho đã được chỉ ra trước đây, và đặc hiệu cho tế bào T CD4 và T CD8 chứ không phải cho DC (Niedzwiecki et al., 2013). Nước bọt của Aedes aegypti hoạt động trên cơ chế điều chỉnh các tế bào của hệ thống miễn dịch khác có lợi cho sự lây nhiễm CHIKV. Tuy nhiên, người ta vẫn chưa xác định rõ những thành phần nào có thể liên quan đến sự lây nhiễm này. Gần đây, Wichit et al. (2017) đã cho thấy rằng Ae. saliva aegypti tạo điều kiện thuận lợi cho sự nhân lên của CHIKV dẫn đến số lượng ngày càng tăng của vi rút trong nguyên bào sợi trong da người, bên cạnh đó nó còn làm giảm gen cảm ứng IFN trong các tế bào bị nhiễm CHIKV thông qua JAK-STAT. Trong số các ổ chứa để lan truyền vi rút, nước bọt của Ae. aegypti gây ra bạch cầu trung tính tại vị trí vết cắn theo cơ chế phụ thuộc vào việc sản xuất CXCL2, với sự tiết IL-1b và CCL-2 sau đó dẫn đến tích tụ bạch cầu trung tính bằng cách huy động trực tiếp các tế bào dòng tủy ( Pingen và cộng sự, 2016).
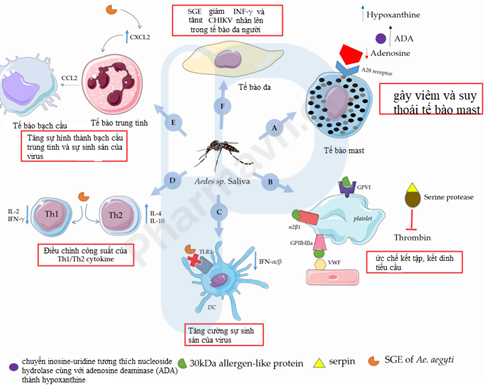
Hình 3. Vai trò điều hòa miễn dịch của Aedes sp. nước bọt trên nhiễm trùng vi rút ở người.
(A) Ae. Aegypti, trong nước bọt inosine-uridine biến nucleoside hydrolase cùng với adenosine deaminase (ADA) chuyển đổi adenosine thành hypoxanthine, do đó ngăn ngừa sản xuất cytokine gây viêm và suy thoái tế bào mast. (B) Protein tương tự chất gây dị ứng 30 kDa, là một protein liên kết collagen có tác dụng ức chế kết tập, kết dính tiểu cầu và serpin ức chế protease nội sinh, chất quan trọng trong việc điều hòa đông máu. (C) Chiết xuất từ nước bọt (SGE) của Aedes sp. giảm biểu hiện của TLR3 và giảm mức IFN-a/b làm tăng sự nhân lên của vi rút. (D) SGE của Ae. aegypti điều chỉnh phản ứng Th1/Th2 có lợi cho sự lây nhiễm CHIKV. (E) Ae. saliva aegypti làm tăng dòng chảy của bạch cầu trung tính đến vết cắn cục bộ bằng cách sản xuất CXCL2, với các bạch cầu trung tính tích lũy sau đó và huy động các tế bào dòng tủy, chúng đóng vai trò là ổ chứa cho sự lan truyền của vi rút. (F) SGE của Ae. Aegypti làm tăng sự sao chép CHIKV trong các nguyên bào sợi của da người và điều chỉnh giảm gen cảm ứng IFN interferon trong các tế bào bị nhiễm CHIKV thông qua JAK-STAT. Hình 3 sử dụng các yếu tố từ www.servier.com.
Ngoài ra, các thành phần của quá trình điều hòa miễn dịch của miRNA có trong nước bọt của Aedes có thể điều chỉnh nhiễm trùng của vi rút. Maharaj và cộng sự. (2015) đã thử nghiệm các loại miRNA khác nhau có trong nước bọt của muỗi nhiễm vi rút, bao gồm miR – 184, miR-12, miR-375 miR-125 và miR-2490. Trong nghiên cứu này, các miRNA này được làm bất hoạt để đánh giá tầm quan trọng của chúng đối với sự sao chép vi rút. Việc làm bất hoạt các miRNA này thúc đẩy sự giảm tốc độ sao chép của vi rút, cho thấy rằng sự hiện diện của các miRNA này điều chỉnh sự sao chép vi rúthoặc kích hoạt các tế bào của hệ thống miễn dịch (Maharaj và cộng sự, 2015).
- Điều trị:
Hiện nay chưa có vaccine ngăn ngừa hay thuốc điều trị cho bệnh chikugunya. Cho đến nay, đã có các vaccine chikugunya đang được thử nghiệm pha I hoặc pha II cho thấy tiềm năng, các vaccine này thuộc các nhóm khác nhau bao gồm vaccine bất hoạt (inactivated vaccine), vaccine tiểu phần (subunit vaccine), vaccine nhược độc (live-attenuated vaccine), vaccine tái tổ hợp (recombinant virus-vectored vaccine), vaccine vỏ virus (virus-like particle vaccine), vaccine khảm (chimeric vaccine) và vaccine nucleic acid. Chẳng hạn, Vogl et al., 2013, Saraswat et al., 2016 đã nỗ lực tối ưu hệ thống biểu hiện nấm men Pichia pastoris để phát triển vaccine vỏ virus cho chikugunya. Goyal et al., 2018 đã phát triển mRNA vaccine dựa trên chỉnh sửa mRNA mã hoá cho cấu trúc polyprotein của virus chikugunya, vaccine này đã cho thấy đáp ứng miễn dịch tốt trên chuột.
Khi bị nhiễm chikugunya, chỉ được điều trị triệu chứng:
- Cho nghỉ ngơi đầy đủ.
- Uống nhiều nước để tránh mất nước.
- Giảm đau và hạ sốt bằng các thuốc như acetaminophen hoặc paracetamol.
- Không sử dụng aspirin và các loại thuốc kháng viêm non-steroid.
- Hỏi ý kiến bác sĩ nếu đang sử dụng các thuốc khác.
- Nếu bị nhiễm chikugunya, tránh bị muỗi đốt trong tuần đầu tiên mắc bệnh để tránh truyền virus từ muỗi cho người khác.
- Ngăn ngừa
Các biện pháp để phòng ngừa nhiễm vi rút chikugunya:
- Cách hiệu quả nhất là tránh bị muỗi đốt.
- Dùng thuốc chống muỗi. Nên sử dụng thuốc chống muỗi được phê duyệt bởi EPA (Environmental Protection Agency) được chứng nhận về an toàn và hiệu quả cho cả phụ nữ mang thai và cho con bú, gồm các thành phần chứa DEET, tinh dầu bạch đàn chanh, Picaridin, Para-menthane-diol (PMD), 2-undecanone hoặc IR3535. Đọc kỹ hướng dẫn trên nhãn sản phẩm để tìm hiểu về các biện pháp phòng ngừa cần được thực hiện và thời gian thuốc có tác dụng. Nếu sử dụng kem chống nắng, thoa kem trước rồi mới đến thuốc chống muỗi.
- Mặc áo dài tay và quần dài.
- Đối với trẻ em, cần cho mặc kín. Chỉ sử dụng loại thuốc chống muỗi có nồng độ thấp DEET cho trẻ em. Thoa DEET lên vùng da tiếp xúc (không bôi lên mắt và miệng) và lên quần áo, không thoa lên các vết cắt hoặc vết thương hở. Không thoa bên dưới quần áo. Không để trẻ em tự thoa thuốc. Thoa thuốc vào tay rồi xoa cho trẻ. Không thoa thuốc vào vùng mắt, miệng hoặc bàn tay của trẻ và sử dụng cẩn thận quanh vùng tai. Không thoa DEET cho trẻ sơ sinh (có thể sử dụng màn chống muỗi bên trên địu em bé) hoặc thoa tinh dầu bạch đàn chanh cho trẻ dưới 3 tuổi.
- Khử trùng trang phục và vật dụng bằng permethrin, không sử dụng permethrin trực tiếp lên da.
- Sử dụng máy điều hòa không khí hoặc màn che cửa sổ/màn che cửa ra vào, đóng kín cửa để ngăn muỗi vào nhà.
Ngoài ra, cần ngăn ngừa muỗi sinh sản bằng cách trút bỏ sạch nước trong những vật dụng chứa nước ít nhất mỗi tuần một lần. Khi đi du lịch, nên chọn chỗ nghỉ có điều hòa hoặc màn che cửa sổ/màn che cửa ra vào, mắc màn nếu ngủ ngoài trời hay nơi không có màn che.
Tóm lại, để ngăn ngừa nhiễm virus chikugunya, cần thực hiện tốt các biện pháp phòng tránh bị muỗi đốt khi ở trong nhà cũng như bên ngoài và hạn chế sự sinh sản của muỗi.
TLTK:
- https://www.cdc.gov/chikungunya/
- https://www.who.int/news-room/fact-sheets/detail/chikungunya
- Monteiro VVS, Navegantes-Lima KC, de Lemos AB, da Silva GL, de Souza Gomes R, Reis JF, Rodrigues Junior LC da Silva OS, Romão PRT and Monteiro MC (2019). Aedes–Chikungunya Virus Interaction: Key Role of Vector Midguts Microbiota and Its Saliva in the Host Infection.
Gao, S., Song, S., & Zhang, L. (2019). Recent Progress in Vaccine Development Against Chikungunya Virus. Frontiers in microbiology, 10, 2881. https://doi.org/10.3389/fmicb.2019.02881