Ceftolozane/tazobactam
ThS. DS. Trịnh Thị Thanh
Ceftolozane/tazobactam là một phối hợp của:
Ceftolozane: kháng sinh thuộc nhóm cephalosporin thế hệ mới, được phê duyệt bởi FDA năm 2014, EMC năm 2015 và Cục Quản lý Dược VN năm 2020 và
Tazobactam: 1 chất ức chế enzyme β-lactamase (phân hủy vòng β-lactam)
Cơ chế hoạt động
Ceftolozane thuộc nhóm cephalosporin, diệt khuẩn thông qua gắn kết với các protein gắn penicillin (PBP) dẫn đến ức chế sự tổng hợp thành tế bào vi khuẩn và sự chết của tế bào sau đó.
Tazobactam là chất ức chế β-lactamase dùng để bảo vệ ceftolozane khỏi đề kháng của vi khuẩn.
Đối với vi khuẩn đề kháng thuốc:
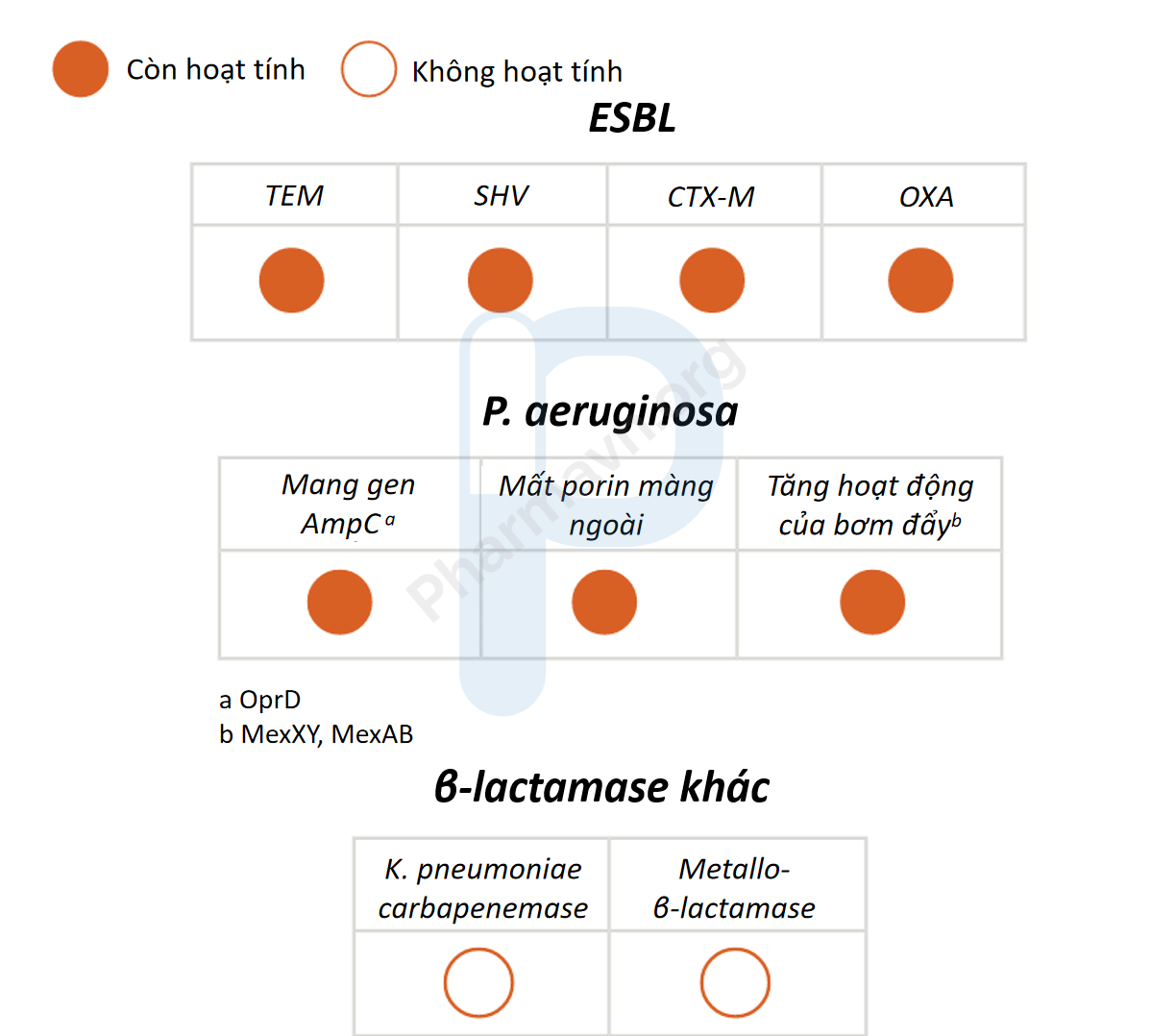
Ceftolozane/tazobactam đã được chứng minh hoạt tính in vitro chống lại vi khuẩn Enterobacteriaceae với sự hiện diện của một số β-lactamase phổ rộng (ESBL) và các β-lactamase khác và chống lại các chủng Pseudomonas aeruginosa với một số cơ chế kháng thuốc nhất định.
Trong các thử nghiệm lâm sàng, một số (không phải tất cả) chủng E. coli và K. pneumoniae tiết β-lactamase nhạy cảm với Ceftolozane/tazobactam (MIC ≤2 mcg/mL)
ZERBAXA không có hoạt tính trên vi khuẩn sinh KPC (K. pneumoniae carbapenemase) và metallo-β-lactamase.
Chỉ định
Bảng 1: Chỉ định và liều dùng Ceftolozane/tazobactam
| Chỉ định | Liều dùng | Thời gian truyền | Thời gian điều trị |
| Nhiễm khuẩn ổ bụng phức tạp (cIAI)* | 1,5g (Ceftolozane 1g + Tazobactam 0,5g) mỗi 8 giờ |
1 giờ | 4-14 ngày |
| Nhiễm khuẩn đường tiết niệu phức tạp (cUTI), bao gồm viêm thận-bể thận | 1,5g (Ceftolozane 1g + Tazobactam 0,5g) mỗi 8 giờ |
1 giờ | 7 ngày |
| Viêm phổi mắc phải trong bệnh viện (HABP)/ Viêm phổi liên quan đến thở máy (VABP) (Chưa được Cục QLD VN phê duyệt) |
3g (Ceftolozane 2g + Tazobactam 1g) mỗi 8 giờ |
1 giờ |
8-14 ngày |
Lưu ý: Chỉ sử dụng Ceftolozane/tazobactam để điều trị nhiễm khuẩn đã được xác định hoặc rất nghi ngờ là gây ra bởi các vi khuẩn nhạy cảm.
Tác dụng phụ
| Hệ thống/ Cơ quan | Thường gặp (1-10%) | Ít gặp (0,1-1%) |
| Máu và hệ bạch huyết | Tăng tiểu cầu | Thiếu máu |
| Chuyển hóa và dinh dưỡng | Giảm kali máu | Tăng đường huyết, giảm magnesi máu, giảm phosphate máu |
| Tâm thần | Lo âu, mất ngủ | |
| Hệ thần kinh | Nhức đầu, chóng mặt | Đột quỵ do thiếu máu cục bộ |
| Tim mạch | Hạ huyết áp | Rung nhĩ, nhịp tim nhanh, đau thắt ngực, viêm tĩnh mạch, huyết khối tĩnh mạch |
| Hô hấp | Khó thở | |
| Tiêu hóa | Buồn nôn, nôn, tiêu chảy, táo bón, đau bụng | Viêm dạ dày, căng tức bụng, khó tiêu, đầy hơi, liệt ruột |
| Da và mô dưới da | Phát ban | Mày đay |
| Thận và tiết niệu | Suy thận | |
| Rối loạn khác | Sốt, phản ứng tại chỗ tiêm truyền | |
| Kết quả xét nghiệm | Tăng men gan | Xét nghiệm Coombs dương tính |
Tương tác thuốc
https://www.drugs.com/drug-interactions/ceftolozane-tazobactam.html
Đối tượng đặc biệt
Suy thận
Cần chỉnh liều đối với bệnh nhân có ClCr ≤ 50ml/phút.
Đối với những bệnh nhân có thay đổi chức năng thận, theo dõi ClCr ít nhất hàng ngày và điều chỉnh liều Ceftolozane/tazobactam tương ứng
Bảng 2: Liều Ceftolozane/tazobactam ở bệnh nhân suy thận
| ClCr* | cIAI và cUTI | HABP/VABP |
| 30-50 ml/phút | 750mg (500mg và 250mg) mỗi 8 giờ | 1,5g (1mg và 0,5mg) mỗi 8 giờ |
| 15-29 ml/phút | 375mg (250mg và 125mg) mỗi 8 giờ | 750mg (500mg và 250mg) mỗi 8 giờ |
| Bệnh thận giai đoạn cuối đang được thẩm phân máu | Liều nạp: 750mg (500mg và 250mg).
Liều duy trì: 150mg (100mg và 50mg) mỗi 8 giờ trong thời gian điều trị còn lại. (Vào những ngày thẩm phân máu, dùng liều này ở thời gian sớm nhất có thể sau khi hoàn thành thẩm phân) |
Liều nạp: 2,25g (1,5g và 0,75g).
Liều duy trì: 450mg (300mg và 150mg) mỗi 8 giờ trong thời gian điều trị còn lại. (Vào những ngày thẩm phân máu, dùng liều này ở thời gian sớm nhất có thể sau khi hoàn thành thẩm phân) |
| * ClCr ước tính bằng công thức Cockcroft-Gault
Tất cả liều Ceftolozane/tazobactam được truyền tĩnh mạch trong 1 giờ |
||
Suy gan
Không cần thiết điều chỉnh liều ở bệnh nhân suy gan
Trẻ em
Độ an toàn và hiệu quả của Ceftolozane/tazobactam ở trẻ em và thiếu niên dưới 18 tuổi chưa được xác định
Người cao tuổi
Trong một phân tích dược động học quần thể về Ceftolozane/tazobactam, không quan sát thấy xu huớng thay đổi AUC có ý nghĩa lâm sàng liên quan đến tuổi. Không khuyến cáo điều chỉnh liều dựa trên giới tính.
Phụ nữ có thai
Không có dữ liệu về việc sử dụng Ceftolozane/tazobactam ở phụ nữ mang thai. Chỉ nên sử dụng thuốc này trong khi mang thai khi lợi ích vượt trội hơn nguy cơ có thể xảy ra.
Phụ nữ cho con bú
Chưa rõ liệu Ceftolozane/tazobactam có được bài tiết vào sữa mẹ hay không. Phải quyết định hoặc ngừng cho con bú hoặc ngừng/tránh điều trị bằng Ceftolozane/tazobactam, có tính đến lợi ích của việc cho con bú đối với trẻ và lợi ích điều trị đối với người mẹ.
Dạng bào chế, cách dùng, bảo quản
Dạng bào chế:
Bột pha dung dịch đậm đặc để pha dung dịch tiêm truyền
Bột màu trắng đến hơi vàng, sau khi pha tạo thành dung dich trong suốt, không màu đến hơi vàng.
Chuẩn bị dung dịch:
Pha lọ thuốc bột với 10ml nước cất pha tiêm hoặc NaCl 0,9% và lắc nhẹ để hòa tan. Thể tích cuối cùng khoảng 11,4ml. LƯU Ý: DUNG DỊCH ĐÃ PHA KHÔNG DÙNG ĐỂ TIÊM TRỰC TIẾP
Để chuẩn bị liều dùng cần thiết, rút thể tích thích hợp được xác định từ Bảng 3 khỏi lọ đã pha. Cho thể tích đã rút vào một chai/túi dịch truyền chứa 100ml NaCl 0,9% hoặc Glucose 5%. Với liều trên 1,5g, hoàn nguyên lọ thuốc thứ hai tương tự lọ đầu tiên, rút thể tích thích hợp và thêm vào cùng một chai/túi dịch truyền.
Bảng 3: Chuẩn bị liều dùng
| Liều Ceftolozane/tazobactam |
Thể tích cần rút từ lọ pha |
| 3g (2g và 1g) | 2 lọ x 11,4ml (toàn bộ chất chứa trong 2 lọ) |
| 2,25g (1,5g và 0,75g) | Lọ thứ nhất 11,4ml (toàn bộ chất chứa trong lọ) và lọ thử hai 5,7ml |
| 1,5g (1mg và 0,5mg) | 11,4ml (toàn bộ chất chứa trong lọ) |
| 750mg (500mg và 250mg) | 5,7ml |
| 450mg (300mg và 150mg) | 3,5ml |
| 375mg (250mg và 125mg) | 2,9ml |
| 150mg (100mg và 50mg) | 1,2ml |
Bảo quản:
Dung dịch Ceftolozane/tazobactam sau khi hoàn nguyên có thể giữ trong 1 giờ trước khi chuyển sang và pha loãng trong chai/ túi dịch truyền thích hợp.
Sau khi pha loãng với dung dịch NaCl 0,9% hoặc Glucose 5%, Ceftolozane/tazobactam ổn định trong 24 giờ khi được bảo quản ở nhiệt độ phòng hoặc 7 ngày khi được bảo quản trong tủ lạnh ở 2–8 oC.
Chống chỉ định:
Chống chỉ định dùng Ceftolozane/tazobactam ở bệnh nhân bị:
- Quá mẫn với hoạt chất hoặc với bất kỳ tá dược nào của thuốc
- Quá mẫn với bất kỳ thuốc kháng sinh nào nhóm cephalosporin
- Quá mẫn nặng (ví dụ phản ứng phản vệ, phản ứng da nặng) với bất kỳ thuốc kháng sinh nhóm β-lactam khác (như penicillin hoặc carbapenem).
Cảnh báo và thận trọng khi dùng thuốc
Suy chức năng thận
Giảm hiệu quả của Ceftolozane/tazobactam đã được quan sát ở bệnh nhân có ClCr nền từ 30-50 mL/phút.
Cần theo dõi thường xuyên bất kỳ thay đổi nào về chức năng thận đối với bệnh nhân bị suy thận ban đầu trong khi điều trị và nên điều chỉnh liều Ceftolozane/tazobactam
khi cần thiết.
Phản ứng quá mẫn
Phản ứng quá mẫn (phản vệ) nghiêm trọng và đôi khi gây tử vong đã được báo cáo ở những bệnh nhân dùng thuốc kháng sinh nhóm β-lactam. Trước khi bắt đầu điều trị bằng Ceftolozane/tazobactam, cần hỏi kỹ tiền sử phản ứng quá mẫn với cephalosporin, penicillin hoặc β-lactam khác, cần thận trọng do sự mẫn cảm chéo đã được xác định. Nếu xảy ra phản ứng phản vệ với Ceftolozane/tazobactam, ngừng dùng thuốc và tiến hành điều trị thích hợp.
Tiêu chảy liên quan với Clostridium difficile (CDAC)
Tiêu chảy liên quan với Clostridium difficile đã được báo cáo gần như đối với tất cả các thuốc kháng khuẩn dùng đường toàn thân, bao gồm cả Ceftolozane/tazobactam. Mức độ nặng của CDAC có thể dao động từ nhẹ đến đe dọa tính mạng. Cần khai thác kỹ tiền sử sử dụng thuốc vì CDAC có thể xảy ra sau 2 tháng sau khi điều trị kháng sinh.Trong những trường hợp xác định CDAC, ngừng điều tri bằng Ceftolozane/tazobactam và nên xem xét sử dụng các biện pháp hỗ trợ cùng với điều trị đặc hiệu đối với Clostridium difficile.
Sự phát triển của vi khuẩn kháng thuốc
Việc kê đơn Ceftolozane/tazobactam khi không có bằng chứng nhiễm khuẩn hoặc không có nghi ngờ nhiều về nhiễm trùng không những không đem lại lợi ích cho bệnh nhân mà còn có nguy cơ phát triển vi khuẩn kháng thuốc.
Nghiệm pháp kháng huyết thanh trực tiếp (nghiệm pháp Coombs) và nguy cơ tiềm ẩn thiếu máu tán huyết
Sự phát triển của một xét nghiệm kháng thể globulin dương tính trực tiếp (DAGT) có thể xảy ra trong quá trình điều trị với Ceftolozane/tazobactam. Tỷ lệ biến đổi huyết thanh DAGT ở bệnh nhân dùng Ceftolozane/tazobactam là 0,2% trong các thử nghiệm lâm sàng. Trong các nghiên cứu lâm sàng, không có bằng chứng tan máu ở bênh nhân phát triển DAGT dương tính khi điều trị.
Hàm lượng Natri
Mỗi lọ Ceftolozane/tazobactam chứa 10mmol (230mg) natri. Lọ đã pha với 10ml dung dịch NaCl 0,9% (dung dịch muối bình thường) để tiêm có chứa 11,5mmol (265mg) natri. Điều này cần được xem xét trong khi điều trị cho bệnh nhân chế độ ăn kiêng có kiểm soát.
Hướng dẫn lâm sàng
Theo Hướng dẫn của IDSA về điều trị nhiễm khuẩn do vi khuẩn Gram âm đa kháng thuốc 2020, Ceftolozane/tazobactam được khuyến cáo cho điều trị vi khuẩn Pseudomonas aeruginosa kháng thuốc khó trị – DRT Pseudomonas).
Xem thêm tại https://pharmavn.org/huong-dan-cua-dieu-tri-nhiem-khuan-khang-thuoc.html
Thử nghiệm lâm sàng
Hiệu quả trong điều trị Nhiễm khuẩn niệu phức tạp (cUTI)
Điều trị Ceftolozane/tazobactam trong 7 ngày so với levofloxacin ở người lớn bị nhiễm trùng đường tiết niệu phức tạp, bao gồm 82% bị viêm bể thận, cải thiện kết quả (giải quyết hoàn toàn hoặc cải thiện rõ rệt các triệu chứng lâm sàng và tỷ lệ tiệt trừ vi khuẩn) 5 đến 9 ngày sau khi bắt đầu điều trị (82,6% so với 79,7%) trong phân nhóm bệnh nhân không có mầm bệnh kháng levofloxacin ban đầu (N = 588), theo một thử nghiệm ngẫu nhiên (N = 1068)
Hiệu quả trong điều trị Nhiễm khuẩn ổ bụng có phức tạp cIAI (phối hợp với metronidazole)
Ceftolozane/tazobactam kết hợp với metronidazole trong 4 đến 14 ngày ở người lớn bị nhiễm trùng trong ổ bụng phức tạp không thua kém meropenem về tỷ lệ chữa khỏi (hết hoàn toàn hoặc cải thiện đáng kể các dấu hiệu và triệu chứng) 24 đến 32 ngày sau khi bắt đầu điều trị (83% so với 87,3%) trong 2 thử nghiệm ngẫu nhiên (N = 979). Ở những bệnh nhân với Enterobacteriaceae tiết enzym kháng β-lactamase phổ rộng CTX-M-14/15 (thường liên quan đến Enterobacteriaceae đa kháng), chữa khỏi lâm sàng ở tất cả 13 bệnh nhân đã sử dụng Ceftolozane/tazobactam phối hợp với metronidazole và trong 72,7% của 11 bệnh nhân sử dụng Meropenem.
Hiệu quả trong điều trị HABP/VABP
Ở bệnh nhân thở máy (N=726), tỷ lệ tử vong ở nhóm điều trị Ceftolozane/tazobactam vào ngày thứ 28 là 24% so với 25,3% ở nhóm điều trị meropenem; TD là 1,1 (95% CI = 5,13 -7,39). Tỷ lệ tử vong do tất cả các nguyên nhân trong viêm phổi nhiễm khuẩn bệnh viện liên quan thở máy (vHABP) thấp hơn ở nhóm Ceftolozane/tazobactam so với Meropenem (24,2% (24/99) so với 37% (40/108); TD là 12,8 (95% CI = 0,18 – 24,75). Tỉ lệ chữa khỏi (hết hoặc cải thiện đáng kể các dấu hiệu và triệu chứng của nhiễm trùng) 7-14 ngày sau khi điều trị là 54,4% và 53,3%; TD là 1,1 (95% CI = 6,17 – 8,29) tương ứng với các nhóm điều trị Ceftolozane/tazobactam và Meropenem. Ở bệnh nhân vHABP, tỷ lệ chữa khỏi là 50,5% (50/99) của nhóm Ceftolozane/tazobactam so với 44,4% (48/108) của nhóm Meropenem (TD là 6,1 (95% CI = 7,44 – 19,27)). Bệnh nhân điều trị Ceftolozane 2g/tazobactam 1g hoặc Meropenem 1g mỗi 8 giờ trong 8 đến 14 ngày.

Tài liệu tham khảo
https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/206829s008lbl.pdf
https://www.medicines.org.uk/emc/medicine/31132#PRODUCTINFO
https://www.merckconnect.com/zerbaxa/dosing-administration/
https://www.micromedexsolutions.com/micromedex2/librarian/CS/EC4D50/ND_PR/evidencexpert/ND_P/evidencexpert/DUPLICATIONSHIELDSYNC/58CAE4/ND_PG/evidencexpert/ND_B/evidencexpert/ND_AppProduct/evidencexpert/ND_T/evidencexpert/PFActionId/evidencexpert.IntermediateToDocumentLink?docId=28790-a&contentSetId=30&title=Ceftolozane&servicesTitle=Ceftolozane
https://drugbank.vn/