Nobel hoá học 2020: Tìm hiểu về Crispr/Cas và các cột mốc phát triển
Giải Nobel Hoá học 2020 được trao cho 2 nhà khoa học người Mỹ Jennifer Doudna và Pháp Emmanuelle Charpentier vì những khám phá quan trọng công cụ điều chỉnh bộ gene Crispr/Cas9, hay được ví von đơn giản là ‘cây kéo’ vàng để cắt nối các đoạn gene di truyền.
Cùng tìm hiểu qua về Crispr/Cas và các cột mốc phát triển quan trọng của phát minh này.
Các scandals xung quanh Crispr/cas9 xem tại link sau
CRISPR/Cas9 – Công cụ khởi đầu cho cuộc cách mạng hóa khoa học sự sống
Một trong những điểm hấp dẫn của khoa học là nó không thể đoán trước được – bạn không bao giờ có thể biết trước một ý tưởng hoặc một câu hỏi có thể dẫn đến đâu. Đôi khi trí óc tò mò sẽ dẫn chúng ta đến ngõ cụt, đôi khi nó sẽ gặp phải một mê cung đầy chông gai mà phải mất hàng năm trời mới định hướng được. Nhưng, bây giờ và một lần nữa, khi mở mắt ra, Emmanuelle Charpentier và Jennifer Doudna đã thấy được rằng những bước chân chập chững mà họ đã bước, đã đưa họ tới một chân trời của khả năng không thể kể hết được.
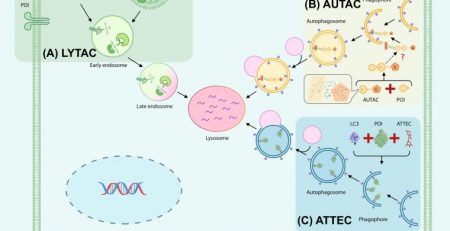
Công cụ chỉnh sửa gen CRISPR-Cas9 là một trong những khám phá đầy bất ngờ với tiềm năng to lớn. Trong quá trình nghiên cứu về vi khuẩn Streptococcus pyogenes, một trong những vi khuẩn gây hại nhiều nhất cho loài người, Emmanuelle Charpentier đã vô tình phát hiện ra một phân tử chưa được biết đến trước đây, tracrRNA. Công trình của cô cho thấy tracrRNA là một phần của hệ thống miễn dịch cổ xưa của vi khuẩn, gọi là CRISPR/Cas, có chức năng tiêu diệu các virus tấn công vào vi khuẩn bằng cách phân cắt DNA của virus. Charpentier công bố khám phá của mình vào năm 2011. Cùng năm, cô bắt đầu hợp tác với Jennifer Doudna, một nhà sinh hóa giàu kinh nghiệm với kiến thức rộng lớn về RNA. Cùng nhau, họ đã thành công trong việc tái tạo lại chiếc kéo phân tử CRISPR/Cas của vi khuẩn trong một ống nghiệm và đơn giản hóa các thành phần phân tử của chiếc kéo để chúng dễ sử dụng hơn. Khi Emmanuelle Charpentier và Jennifer Doudna bắt đầu điều tra hệ thống miễn dịch của vi khuẩn Streptococcus, họ nghĩ rằng họ có thể phát triển một dạng kháng sinh mới. Nhưng không, thay vào đó, họ lại phát hiện ra một công cụ phân tử có thể được sử dụng để tạo những vết cắt chính xác trên DNA, giúp thay đổi các đoạn mã của sự sống một cách dễ dàng.
Ngay sau khi Emmanuelle Charpentier và Jennifer Doudna công bố khám phá ra kéo phân tử CRISPR /Cas9 vào năm 2012, một số nhóm nghiên cứu đã chứng minh rằng công cụ này có thể được sử dụng để sửa đổi bộ gen tế bào của cả chuột và người, dẫn đến sự bùng nổ mạnh mẽ của công nghệ chỉnh sửa gen. Trước đây, việc thay đổi các gen trong tế bào, thực vật hoặc sinh vật rất tốn thời gian và đôi khi là không thể. Bằng cách sử dụng kéo phân tử, về nguyên tắc, các nhà nghiên cứu có thể tạo ra những vết cắt ở bất kỳ bộ gen nào họ muốn. Sau đó, sẽ rất dễ dàng để họ viết lại các đoạn mã của sự sống thông qua cơ chế sửa chữa DNA tự nhiên của tế bào.
Vì công cụ gen này rất dễ sử dụng nên hiện nay nó đã được phổ biến rộng rãi trong nghiên cứu cơ bản: Nó được sử dụng để tạo nên các mô hình tế bào và động vật chỉnh sửa gen nhằm mục đích tìm hiểu cách thức các gen khác nhau hoạt động và tương tác, chẳng hạn như trong quá trình bệnh; Trong nông nghiệp, các nhà nghiên cứu đã có thể phát triển các loại cây trồng chống chịu được nấm mốc, sâu bệnh và hạn hán. Trong y học, các thử nghiệm lâm sàng về liệu pháp điều trị ung thư mới đang được tiến hành và ước mơ có thể chữa khỏi các bệnh di truyền sắp trở thành hiện thực. CRIPRS/Cas9 đã trở thành câu chuyện khoa học lớn nhất thập kỷ, đưa ngành khoa học sự sống bước sang một kỷ nguyên mới và mang lại lợi ích lớn nhất cho loài người.
“Có một sức mạnh to lớn trong công cụ di truyền này, nó ảnh hưởng đến tất cả chúng ta. Nó không chỉ tạo nên một cuộc cách mạng trong khoa học cơ bản mà còn tạo ra những cây trồng sáng tạo và sẽ dẫn đến những phương pháp điều trị y tế mới mang tính đột phá.” Dẫn lời từ Claes Gustafsson, chủ tịch Ủy ban Nobel Hóa học.
Thông qua việc khám phá ra CRIPRS/Cas9, Emmanuelle Charpentier và Jennifer Doudna đã phát triển nên một công cụ đưa khoa học sự sống vào một kỷ nguyên mới. Không chỉ họ, mà ngay cả chúng ta cũng bắt đầu nhìn thấy được một chân trời rộng lớn với tiềm năng không thể tưởng tượng được của công cụ chỉnh sửa gen. Có một điều chắc chắn rằng: sớm thôi, những chiếc kéo phân tử này sẽ ảnh hưởng rất nhiều lên tất cả chúng ta. Quan trọng nhất là việc phải đối mặt với các vấn đề đạo đức mới, nhưng bù lại công cụ mới này có thể góp phần giải quyết nhiều thách thức mà nhân loại đang phải đối mặt.
Từ khi cơ chế được khám phá vào năm 1987, đã có nhiều cột mốc quan trọng về sự phát triển của Crispr/Cas9 cho thấy ứng dụng cực kỳ lớn vào nhiều mặt của đời sống.
Các cột mốc quan trọng về phát triển của Crispr/Cas

| Thời gian | Sự kiện | Nhóm tác giả | Vị trí |
| Tháng 12/1987 | Cơ chế CRISPR lần đầu tiên được công bố | Amemura, Ishino, Makino, Nakata, Shinagawa, Takase, Wachi | Osaka University |
| 18/1/2000 | Nhiều trình tự DNA lặp lại được xác định ở các vi khuẩn và vi khuẩn cổ khác, được gọi là ‘các đoạn lặp ngắn được giãn cách đều nhau’ (Short Regularly Spaced Repeats-SRSR) | ||
| Tháng 3/2002 | Thuật ngữ CRISPR-Cas9 được công bố lần đầu tiên | Mojica, Jansen, Embden, Gaastra, Schouls | Utrecht University |
| 2005 | Jennifer Doudna và Jillian Banfield bắt đầu nghiên cứu CRISPR | Doudna, Banfield | University of California Berkeley |
| 1/8/2005 | Các nhà khoa học Pháp đề xuất trình tự đệm CRISPR có thể cung cấp khả năng miễn dịch tế bào chống lại sự lây nhiễm của thực khuẩn thể và làm thoái hóa DNA | ||
| 11/10/2005 | Các nhà nghiên cứu người Mĩ xác định được các họ gen Cas mới giúp bảo vệ vi khuẩn chống lại vi rút xâm nhập | ||
| 23/32007 | Các thí nghiệm lần đầu tiên chứng minh vai trò của CRISPR cùng với gen Cas9 trong việc bảo vệ vi khuẩn chống lại vi rút | ||
| 2008 | Chứng minh DNA là mục tiêu phân tử của hầu hết các hệ thống CRISPR-Cas chứ không phải RNA | ||
| Tháng 2/2008 | Các nhà khoa học sử dụng thuật ngữ “protospacer” để biểu thị chuỗi virus tương ứng với “vùng đệm” trong hệ thống CRISPR-Cas9 | ||
| Tháng 8/2008 | Các nhà khoa học xác định được đặc điểm của con đường xử lý RNA trong hệ thống CRISPR | ||
| Tháng 12/2008 | Các nhà khoa học công bố con đường chống phiên dịch RNA liên quan đến cơ chế CRISPR-Cas | ||
| Năm 2011 | Sự phân loại hệ thống CRISPR-Cas được đề xuất | ||
| Tháng 3/2011 | Emmanuelle Charpentier và Jennifer Doudna hợp tác để nghiên cứu enzym Cas9 | Doudna, Charpentier, Hinek, Hauser | University of California Berkeley, Umea University |
| Tháng 4/2012 | Lần đầu tiên thương mại hóa công nghệ CRISPR-Cas9 | Dupont | |
| Tháng 5/2012 | Nộp đơn đăng ký bằng sáng chế đầu tiên cho công nghệ CRISPR-Cas9 | Doudna, Charpentier | University of California Berkeley, University of Vienna |
| 17/8/2012 | Công bố phương pháp chỉnh sửa gen hoàn toàn mới khai thác hệ thống CRISPR-Cas9 | Jinek, Chylinski, Fonfara, Hauer, Doudna, Charpentier | University of California Berkeley |
| 12/12/2012 | Đơn đăng ký nhanh cho công nghệ CRISPR-Cas9 được nộp cho văn phòng cấp bằng sáng chế Hoa Kỳ | Zhang | Broad Institute, Massachusetts Institute of Technology |
| Tháng 1/2013 | CRISPR-Cas được sử dụng trong chỉnh sửa bộ gen người | ||
| Tháng 1/2013 | CRISPR-Cas được sử dụng để chỉnh sửa bộ gen của cá sọc vằn | ||
| Tháng 2/2013 | CRISPR-Cas được hiển thị để lập trình ức chế và kích hoạt sự phiên mã gen | Bikard, Murrafini | Rockefeller University |
| Tháng 3/2013 | CRISPR-Cas được sử dụng để chỉnh sửa bộ gen của Saccharomyces cerevisiae, một loài nấm men được dùng trong làm bánh, lên men bia, rượu. | ||
| 1/4/2013 | Quá trình điều hòa gen bởi CRISPR-Cas được minh chứng là giúp điều hòa các gen của vi khuẩn nội sinh. | ||
| Tháng 8/2013 | CRISPR-Cas được sử dụng để xây dựng bộ gen của chuột | ||
| Tháng 8/2013 | CRISPR-Cas được sử dụng để xây dựng bộ gen thực vật bao gồm gạo, lúa mì, thuốc lá và lúa mì. | ||
| Tháng 8/2013 | Đặc tính riêng của hệ thống CRISPR-Cas được cải tiến. | ||
| Tháng 3/2015
|
Các nhà khoa học cho rằng sử dụng CRISPR / Cas9 trên tế bào gốc có thể cung cấp nội tạng cho người từ lợn chuyển gen. | Feng, Dai, Mou, Cooper, Shi, Cai | Shenzhen University, University of Pittsburgh Medical Center |
| 26/3/2015 | Các nhà khoa học Hoa Kỳ kêu gọi tự nguyện tạm hoãn trên toàn thế giới về việc sử dụng các công cụ chỉnh sửa bộ gen để sửa đổi các tế bào sinh sản của con người. | Lamphier, Urnov | |
| 15/4/2015
|
Viện Y tế Quốc gia tuyên bố sẽ không tài trợ cho việc sử dụng bất kỳ công nghệ chỉnh sửa bộ gen nào trên phôi người.
|
||
| 22/04/2015 | Hội đồng Đạo đức Sinh học Nuffield của Vương quốc Anh đã thành lập một nhóm công tác mới để xem xét các thể chế chính sách và quy định của quốc gia, quốc tế liên quan đến việc chỉnh sửa bộ gen. | ||
| 1/5/2015 | Báo cáo đầu tiên về các gen được chỉnh sửa trên phôi người đã gây ra cuộc tranh luận đạo đức toàn cầu về công nghệ chỉnh sửa gen. | Huang, Liang, Xu, Zhang | Sun Yat-sen University |
| 2/9/2015 | Các hội đồng nghiên cứu hàng đầu của Vương quốc Anh, bao gồm cả MRC, đã tuyên bố ủng hộ việc sử dụng CRISPR-Cas9 và các kỹ thuật chỉnh sửa bộ gen khác trong nghiên cứu tiền lâm sàng. | ||
| 11/9/2015 | Tập đoàn Hinxton đưa ra một tuyên bố chỉ ra rằng hầu hết các câu hỏi đạo đức, luân lý được nêu ra về CRISPR và chỉnh sửa gen đã được tranh luận trước đây. | ||
| 15/9/2015 | Hội đồng Đạo đức Sinh học Nuffield của Vương quốc Anh đã tổ chức hội thảo đầu tiên để xác định và định nghĩa các câu hỏi về đạo đức liên quan đến sự phát triển trong nghiên cứu chỉnh sửa bộ gen. | ||
| 18/9/2015 | Các nhà khoa học Anh đã xin giấy phép để tiến hành biến đổi gen trên phôi người để nghiên cứu vai trò của các gen trong những ngày đầu tiên của quá trình thụ tinh ở người. | Naikan | Crick Institute |
| 25/9/2015 | Protein mới Cpf1 được tìm thấy, cung cấp phương tiện giúp đơn giản hóa việc chỉnh sửa gen. | Zhang, Zetsche, Gootenberg, Abudayyeh, Slaymaker | Broad Institute, Massachusetts Institute of Technology |
| 5/10/2015 | CRISPR / Cas9 đã biến đổi 60 gen trên phôi lợn, bước đầu tạo ra các cơ quan phù hợp cho việc cấy ghép nội tạng ở người. | Church | Harvard University |
| 6/10/2015 | Ủy ban Đạo đức sinh học Quốc tế của UNESCO đã kêu gọi cấm chỉnh sửa gen trên tế bào mầm của người. | ||
| 16/11/2015
|
Các nhà khoa học Hoa Kỳ đã công bố một kỹ thuật để thay thế các thay đổi do CRISPR / Cas 9 tạo ra. | DiCarlo, Chavez, Dietz, Esvelt, Church | Harvard University, Swiss Federal Institute of Technology in Zurich |
| 23/11/2015 | Các nhà khoa học Mỹ đã biến đổi gen muỗi bằng CRISPR / Cas9 để ngăn chúng mang ký sinh trùng gây bệnh sốt rét. | Gantz, Jasinskiene, Tatarenkova, Fazekas, Macias, Bier, James | University California San Diego, University of California Irvine |
| 1/12/2015 | Hội nghị Thượng đỉnh Quốc tế về Chỉnh sửa gen người đã họp để thảo luận về các vấn đề khoa học, y tế, đạo đức và quản trị liên quan đến những tiến bộ gần đây trong nghiên cứu chỉnh sửa gen người | Baltimore, Doudna, Church, Zhang | US National Academies of Science, Engineering and Medicine |
| 31/12/2015 | Công cụ chỉnh sửa gen – CRISPR được sử dụng thành công để cải thiện chức năng của cơ trên mô hình chuột mắc chứng loạn dưỡng cơ Duchenne | Nelson, Gersbach, Hakim, Ousterout, Thakore | Duke University, Harvard, MIT |
| 6/1/2016 | Các nhà khoa học Mỹ đã công bố phiên bản cải tiến của CRISPR / Cas 9 làm giảm nguy cơ đứt gãy DNA chệch mục tiêu | Kleinstiver, Pattanayak, Prew, Tsai, Nguyen, Zheng, Joung | Harvard University |
| 1/12/2016 | Các nhà khoa học Vương quốc Anh được phép biến đổi gen phôi người bằng CRISPR-Cas 9 | Niakan | Crick Institute |
| 16/5/2016 | Các nhà khoa học Hoa Kỳ công bố kỹ thuật chỉnh sửa cơ sở mới cung cấp các phương tiện để thay đổi bộ gen mà không cần cắt chuỗi kép DNA hoặc lấy mẫu DNA của người hiến tặng | Komor, Kim, Packer, Zuris, Liu | Harvard University |
| 21/6/2016 | 2016: NIH đã “bật đèn xanh” cho thử nghiệm lâm sàng đầu tiên sử dụng công cụ chỉnh sửa gen CRISPR / Cas 9 để điều trị cho bệnh nhân | ||
| 2/2017 | Viện Hàn lâm Khoa học và Y học Quốc gia Hoa Kỳ đã “bật đèn xanh” để tiến hành CRISPR trong các thí nghiệm dòng mầm | ||
| 13/4/2017 | CRISPR được chứng minh là công cụ chẩn đoán nhạy để phát hiện mục tiêu đơn lẻ của phân tử DNA hoặc RNA | Zhang et al. | Institute of Technology, Harvard University, HHMI |
| 13/05/2017 | Nghiên cứu được công bố chứng minh cách CRISPR-CAS9 có thể được sử dụng để loại bỏ HIV ở chuột bị nhiễm bệnh. | Hu et al. | Temple University, University of Pittsburgh |
| 2/8/2017 | Nghiên cứu được công bố chứng minh khả năng chỉnh sửa khiếm khuyết gen trong phôi người được cấy sớm để ngăn ngừa bệnh tim di truyền | ||
| 9/2017 | DNA của phôi người được chỉnh sửa bằng CRISPR-Cas9 để nghiên cứu nguyên nhân vô sinh | Niakan et al. | Crick Instiitute, Oxford |
| 23/9/2017 | Các nhà nghiên cứu Trung Quốc báo cáo việc chỉnh sửa gen liên quan đến bệnh beta-thalassemia, rối loạn máu di truyền, trong phôi người sử dụng kỹ thuật chỉnh sửa cơ sở | Huang et al. | Sun Yat-sen University, Baylor College of Medicine |
| 25/10/2017 | Kỹ thuật CRISPR mới được công bố để chỉnh sửa RNA | ||
| 25/10/2017 | Cải tiến kĩ thuật chỉnh sửa cơ sở được công bố thay cho kỹ thuật CRISPR, cung cấp các phương tiện để thay đổi từng kí tự hóa học của DNA mà không cần phải cắt DNA | Gaudelli, Komor, Rees, Packer, Badran, Bryson, Liu | Massachusetts Institute of Technology, Harvard University |
| 5/1/2018 | Các nhà nghiên cứu nhận ra các kháng thể tồn tại từ trước nhắm vào các protein CAS9 làm tăng khả năng đáp ứng miễn dịch làm suy yếu lợi ích của CRISPR-Cas9 cho liệu pháp gen | ||
| 27/8/2018 | Thử nghiệm lâm sàng về CRISPR-Cas9 đầu tiên ra mắt | Vertex Pharmaceuticals, CRSIPR Therapeutics | |
| 24/11/2018 | Nhà khoa học Trung Quốc công bố những đứa trẻ đầu tiên được chỉnh sửa gen | Jiankui | China |
| 14/12/2018 | Kỹ thuật chỉnh sửa gen mới (CRISPRa) giúp tăng khả năng biểu hiện của gen mục tiêu | ||
| 21/12/2018 | Chỉnh sửa CRISPR-Cas9 đã giúp khôi phục hiệu quả của các thuốc điều trị đầu tay cho bệnh ung thư phổi | ||
| 23/1/2019 | CRISPR-Cas9 được sử dụng để kiểm soát sự di truyền gen ở chuột | ||
| 21/10/2019 | Kỹ thuật chỉnh sửa DNA mới: “prime editing” được công bố | Liu et al. | MIT, Harvard |
| 30/12/2019 | Nhà khoa học Trung Quốc bị kết án vì sử dụng CRISPR-Cas9 ở trẻ sơ sinh | Jiankui | China |
| 4/3/2020 | Bệnh nhân đầu tiên được điều trị chỉnh sửa gen bằng việc đưa trực tiếp CRISPR vào cơ thể | Pennesi | Oregon Health and Science University |
| 7/10/2020 | Giải Nobel Hóa học được trao cho Emmanuelle Charpentier và Jennifer Doudna cho việc phát triển một phương pháp chỉnh sửa gen. | Doudna, Charpentier | University California Berkeley, University of Umea |
Nhóm tác giả:
TS.DS. Phạm Đức Hùng
Nguyễn Thái Minh Trận
Mỹ Ngọc
Đỗ Thị Biển
Lâm Ngọc Kim Trúc
TLTK
- https://cen.acs.org/policy/litigation/Broad-prevails-over-Berkeley-CRISPR/96/web/2018/09
- https://www.sciencemag.org/news/2020/09/latest-round-crispr-patent-battle-has-apparent-victor-fight-continues
- https://www.technologyreview.com/2018/12/11/138290/years-before-crispr-babies-this-man-was-the-first-to-edit-human-embryos/
- https://www.facebook.com/t.nguyen.2016/posts/1087954931651823
- Heidi Ledford, 2019, “Super-precise new CRISPR tool could tackle a plethora of genetic diseases”, naturehttps://www.nature.com/articles/d41586-019-03164-5, 8/10/2020.
- Dennis Normile, 2019, Chinese scientist who produced genetically altered babies sentenced to 3 years in jail, Sciencemag, https://www.sciencemag.org/news/2019/12/chinese-scientist-who-produced-genetically-altered-babies-sentenced-3-years-jail, 8/10/2020.
- “Pro and Con: Should Gene Editing Be Performed on Human Embryos?”, National Geograpic, https://www.nationalgeographic.com/magazine/2016/08/human-gene-editing-pro-con-opinions/, 8/10/2020.
Hình thumbnail 2 nhà khoa học Doudna và Charpentier tại website của tổ chức Nobel